题目内容
17.甲乙两种非金属性质比较,有①甲比乙在相同条件下更容易与氢气化合;②甲单质能与乙的阴离子发生置换反应;③最高价氧化物对应的水化物酸性比较,甲比乙的强;④与一定量某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低.能够说明甲比乙的非金属性强的是( )| A. | ①②③ | B. | ①③④ | C. | ①②⑤ | D. | ①②③④⑤ |
分析 比较元素的非金属性强弱,可从与氢气反应的剧烈程度、单质的氧化性、氢化物的稳定性、最高价氧化物对应水化物的酸性强弱等角度判断,注意不能根据得失电子的多少以及熔沸点的高低等角度判断.
解答 解:①在相同条件下,甲比乙容易与H2化合,可说明甲比乙的非金属性强,故①正确;
②甲单质能与乙的阴离子发生置换反应,则单质的氧化性甲比乙强,可说明甲比乙的非金属性强,故②正确;
③甲的最高价氧化物对应的水化物的酸性比乙的最高价氧化物对应的水化物酸性强,可说明甲比乙的非金属性强,故③正确;
④与某金属反应时甲原子得电子数目比乙的多,不能说明可说明甲比乙的非金属性强,非金属性的强弱只与得电子的能力有关,故④错误;
⑤甲的单质熔沸点比乙的低,属于物理性质,与得失电子的能力无关,不能用来判断非金属性的强弱,故⑤错误.
正确的有①②③,
故选A.
点评 本题考查非金属性的比较,题目难度不大,本题注意把握比较非金属性的角度,注意元素周期律的变化,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
7.化学兴趣小组对某工厂排放的废水取样检测得知废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是( )
| A. | K+、NO3-、OH- | B. | K+、NO3-、SO42- | C. | Na+、Fe3+、Cl- | D. | Na+、CO32-、SO42- |
8.下列各组物质中,互为同系物的是( )
| A. | $\stackrel{234}{92}$U和$\stackrel{238}{92}$U | B. | CO2和干冰 | C. | CH4和CH3CH2CH3 | D. | 正丁烷和异丁烷 |
5.下列说法不正确的是( )
| A. | (CH3)2C═O+HCN→(CH3)2C(OH)CN 属于加成反应 | |
| B. | CH3OH、CH2OHCH2OH、CH2OHCHOHCH2OH是同系物 | |
| C. |  属于取代反应 属于取代反应 | |
| D. | 1molCH3CH3与Cl2完全反应生成六氯乙烷时,消耗Cl26mol |
12.百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧.其主要化学成分的结构简式为: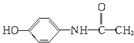 .下列有关该有机物叙述正确的是( )
.下列有关该有机物叙述正确的是( )
 .下列有关该有机物叙述正确的是( )
.下列有关该有机物叙述正确的是( )| A. | 分子式为C8H10NO2 | |
| B. | 其属于α-氨基酸的同分异构体有3种 | |
| C. | 该有机物属于α-氨基酸 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
9.某实验室用的蒸馏水,可以被某种酸严重污染,采用下列几种方法进行检验,其中不可行的是( )
| A. | 取样品,向其中滴加石蕊试液 | B. | 取样品,向其中加入CaCO3粉末 | ||
| C. | 取样品,向其中滴加Ba(NO3)2溶液 | D. | 取样品,向其中滴加Na2CO3溶液 |
15.从海带中提取碘单质,成熟的工艺流程如下:干海带$\stackrel{灼烧}{→}$海带灰$→_{浸泡}^{沸水}$悬浊液$\stackrel{过滤}{→}$滤液$→_{H_{2}O_{2}}^{H+}$碘水$\stackrel{CCl_{4}}{→}$I2的CCl4
溶液$\stackrel{蒸馏}{→}$ I2下列关于海水制碘的说法正确的是( )
溶液$\stackrel{蒸馏}{→}$ I2下列关于海水制碘的说法正确的是( )
| A. | 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 | |
| B. | 含I-的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 | |
| C. | 在碘水中加入几滴淀粉溶液,溶液出现蓝色沉淀 | |
| D. | 碘水加入CCl4得到I2的CCl4溶液,该操作为萃取 |

 .分别写出②和⑦、③和⑧化合产物的电子式
.分别写出②和⑦、③和⑧化合产物的电子式 、
、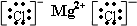 .⑤和⑥的气态氢化物的稳定性NH3>CH4(写化学式).⑦和⑧的最高价氧化物的水化物的酸性HClO4>H2SO4(写化学式).
.⑤和⑥的气态氢化物的稳定性NH3>CH4(写化学式).⑦和⑧的最高价氧化物的水化物的酸性HClO4>H2SO4(写化学式).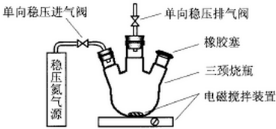 水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.
水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.