题目内容
2.
(1)写出上面元素周期表中元素⑤的名称和符号碳、C.
(2)从①--⑩各元素中,形成化合物种类最多的元素是C;金属性最强的元素是K;非金属性最强的元素是Cl;最不活泼的元素是Ar(写元素符号).
(3)写出④最高价氧化物的水化物与②的最高价氧化物的水化物的溶液反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)①和⑧两种元素的单质混合在光照下能化合,写出该化合产物的电子式
 .分别写出②和⑦、③和⑧化合产物的电子式
.分别写出②和⑦、③和⑧化合产物的电子式 、
、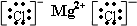 .⑤和⑥的气态氢化物的稳定性NH3>CH4(写化学式).⑦和⑧的最高价氧化物的水化物的酸性HClO4>H2SO4(写化学式).
.⑤和⑥的气态氢化物的稳定性NH3>CH4(写化学式).⑦和⑧的最高价氧化物的水化物的酸性HClO4>H2SO4(写化学式).(5)在前人经验的基础上,系统归纳总结出实用并有很强理论性的元素周期律和元素周期表的是俄国伟大的化学家门捷列夫.
分析 由元素在周期表中的位置可知,①为H,②为Na,③为Mg,④为Al,⑤为C,⑥为N,⑦为S,⑧为Cl,⑨为Ar,⑩为K,然后利用元素及其单质、化合物的性质来解答.
解答 解:(1)由元素在周期表中的位置可知,⑤为C,名称为碳,
故答案为:碳;C;
(2)在已经发现的3000多万种物质中,有机物占90%以上,有机物是含有碳元素的化合物,所以从①--⑩各元素中,形成化合物种类最多的元素是碳元素,同周期从左向右元素的金属性减弱、非金属性增强,同主族从上到下元素的金属性增强、非金属性减弱,上述元素中K的金属性最强,Cl的非金属性最强,稀有气体Ar原子最外层为稳定结构,化学性质最不活泼,
故答案为:C;K;Cl;Ar;
(3)②位于第三周期第ⅠA族,为Na元素,对应的最高价氧化物的水化物为NaOH,为强碱,④是两性氧化物的元素是铝元素,铝的最高价氧化物对应的水化物是氢氧化铝,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)①为H,⑧为Cl,两种元素的单质混合在光照下能化合生成氯化氢,氯化氢为共价化合物,氯原子最外层达到8个电子稳定结构,氯化氢的电子式为: ,②和⑦化合产物为硫化钠,是钠离子和硫离子形成的离子化合物,硫化钠的电子式为:
,②和⑦化合产物为硫化钠,是钠离子和硫离子形成的离子化合物,硫化钠的电子式为: ,③和⑧化合产物为氯化镁,是离子化合物,由氯离子和镁离子构成,氯化镁电子式为
,③和⑧化合产物为氯化镁,是离子化合物,由氯离子和镁离子构成,氯化镁电子式为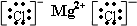 ,非金属性越强,气态氢化物越稳定,⑤为C,⑥为N,非金属性N>C,则气态氢化物的稳定性:NH3>CH4,元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;同一周期元素,其非金属性随着原子序数增大而增强,⑦为S,⑧为Cl,所以酸性HClO4>H2SO4,
,非金属性越强,气态氢化物越稳定,⑤为C,⑥为N,非金属性N>C,则气态氢化物的稳定性:NH3>CH4,元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;同一周期元素,其非金属性随着原子序数增大而增强,⑦为S,⑧为Cl,所以酸性HClO4>H2SO4,
故答案为: ;
; ;
;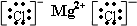 ;NH3>CH4;HClO4>H2SO4;
;NH3>CH4;HClO4>H2SO4;
(5)1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,
故答案为:俄;门捷列夫.
点评 本题考查元素周期表和元素周期律,熟悉元素在周期表中的位置及元素、化合物的性质是解答本题的关键,题目难度中等,注意化学用语的使用来解答.

| A. | 在标准状况下,22.4 L苯所含的分子数为NA | |
| B. | 0.1 mol/L NaOH溶液所含的Na+数为0.1NA | |
| C. | 在常温常压下,11.2 L CH4所含的氢原子数为2NA | |
| D. | 在标准状况下,14 g氮气所含的核外电子数为7NA |
| A. | 氯化铁溶液 饱和溴水 | B. | 碳酸钠溶液 饱和溴水 | ||
| C. | 酸性高锰酸钾溶液 饱和溴水 | D. | 酸性高锰酸钾溶液 氯化铁溶液 |
| A. | ①②③ | B. | ①③④ | C. | ①②⑤ | D. | ①②③④⑤ |
| A. | 50mL烧杯 | B. | 25mL量筒 | C. | 100mL容量瓶 | D. | 500mL量杯 |
| A. | 乙烷 | B. | 正戊烷 | C. | 正丁烷 | D. | 新戊烷 |
| A. | 一氯乙烷的结构式CH3Cl | B. | 乙醇分子的比例模型: | ||
| C. | N2的电子式: | D. | 苯的分子式C6H6 |
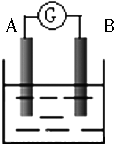 如图为原电池装置示意图:
如图为原电池装置示意图: 根据题意回答下列问题
根据题意回答下列问题 .
. .
.