题目内容
最近研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
A、羰基硫的电子式为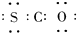 |
| B、羰基硫分子的中心原子为氧 |
| C、羰基硫中三个原子处于同一直线上 |
| D、羰基硫是非极性分子 |
考点:电子式,判断简单分子或离子的构型,极性分子和非极性分子
专题:化学用语专题,化学键与晶体结构
分析:A.根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式;
B.结合二氧化碳分子结构,可知碳原子为中心原子,分别于氧原子和硫原子形成共价键;
C.根据二氧化碳的结构判断羰基硫的结构;
D.极性分子中正负电荷的中心不重合.
B.结合二氧化碳分子结构,可知碳原子为中心原子,分别于氧原子和硫原子形成共价键;
C.根据二氧化碳的结构判断羰基硫的结构;
D.极性分子中正负电荷的中心不重合.
解答:
解:A.羰基硫的电子式为: ,故A错误;
,故A错误;
B.羰基硫分子的中心原子为碳,故B错误;
C.二氧化碳结构对称,所以羰基硫也是直线型分子,但2个极性键的极性不等,所以中正负电荷的中心不重合,是极性分子,故C正确;
D.羰基硫正负电荷的中心不重合,是极性分子,故D错误;
故选:C.
 ,故A错误;
,故A错误;B.羰基硫分子的中心原子为碳,故B错误;
C.二氧化碳结构对称,所以羰基硫也是直线型分子,但2个极性键的极性不等,所以中正负电荷的中心不重合,是极性分子,故C正确;
D.羰基硫正负电荷的中心不重合,是极性分子,故D错误;
故选:C.
点评:本题考查了电子式的书写、非金属性强弱的判断、金属的电化学腐蚀等知识,题目难度中等,熟悉二氧化碳的结构,学会迁移应用时解题关键,注意掌握电子式的书写方法.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ | ||||
B、NH4HCO3溶于过量的NaOH溶液中:HCO
| ||||
C、稀H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO
| ||||
D、AgNO3溶液中加入过量的氨水:Ag++NH3?H2O═AgOH↓+NH
|
已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是( )
| A、依据其结构判断该含氧酸为强酸 |
| B、O原子是sP3杂化 |
| C、该分子为直线型非极性分子 |
| D、该分子的电子式是H:O:Cl |
铅蓄电池用途极广,电解液为30% H2SO4溶液,电池的总反应式可表示为:
Pb(s)+PbO2(s)+2H2SO4(aq)
2PbSO4(s)+2H2O(l),下列有关叙述正确的是( )
Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
| A、放电时电解液的密度不断增大 |
| B、放电时电子从Pb通过导线转移到PbO2 |
| C、充电时Pb极与外电源的正极相连 |
| D、充电时PbO2电极发生还原反应,Pb电极上发生氧化反应 |
将绿矾晶体加强热,除生成水蒸气以外,还发生如下反应:2FeSO4═Fe2O3+SO2↑+SO3↑,如将生成的混合气体通过BaCl2溶液,应发生的现象有( )
| A、一定产生BaSO4沉淀 |
| B、一定产生BaSO3沉淀 |
| C、一定有BaSO4沉淀 和BaSO3沉淀 |
| D、一定有SO3逸出 |
下列有关过滤实验的操作中不 正确的是( )
| A、过滤操作中,玻璃棒与三层滤纸相互接触 |
| B、过滤操作中,漏斗颈与烧杯内壁相互接触 |
| C、过滤操作中,玻璃棒与烧杯口相互接触 |
| D、为加快过滤,使用玻璃棒搅动漏斗里的液体 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,1.8 g水中所含有氧原子数目为0.1NA |
| B、常温常压下,2.24L CO2气体中含氧原子数目为0.2NA |
| C、0.1 mol/LCuCl2溶液中,含有Cl-离子的数目为0.2NA |
| D、常温常压下,2.3 g Na+中含有的电子数为NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.5moL/L、2L的AlCl3溶液中含有氯离子数为NA |
| B、25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA |
| C、在常温常压下,11.2 L Cl2含有的分子数为0.5 NA |
| D、1 L 0.1 mol/LNaCl溶液中所含的Na+ 的电子数为1.1NA |