题目内容
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,1.8 g水中所含有氧原子数目为0.1NA |
| B、常温常压下,2.24L CO2气体中含氧原子数目为0.2NA |
| C、0.1 mol/LCuCl2溶液中,含有Cl-离子的数目为0.2NA |
| D、常温常压下,2.3 g Na+中含有的电子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.水的摩尔质量为18g/mol,1.8g水中含有0.1mol水,含有0.1mol氧原子;
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量;
C.缺少氯化铜溶液的体积,无法计算溶液中氯离子的数目;
D.钠离子含有10个电子,2.3g钠的物质的量为0.1mol,含有1mol电子.
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量;
C.缺少氯化铜溶液的体积,无法计算溶液中氯离子的数目;
D.钠离子含有10个电子,2.3g钠的物质的量为0.1mol,含有1mol电子.
解答:
解:A.1.8g水中含有0.1mol水,0.1mol水中含有0.1mol氧原子,所含有氧原子数目为0.1NA,故A正确;
B.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L二氧化碳的物质的量,故B错误;
C.没有告诉氯化铜溶液的体积,无法计算溶液中氯离子的物质的量,故C错误;
D.2.3g钠的物质的量为0.1mol,0.1mol钠离子中含有1mol电子,含有的电子数为NA,故D正确;
故选AD.
B.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L二氧化碳的物质的量,故B错误;
C.没有告诉氯化铜溶液的体积,无法计算溶液中氯离子的物质的量,故C错误;
D.2.3g钠的物质的量为0.1mol,0.1mol钠离子中含有1mol电子,含有的电子数为NA,故D正确;
故选AD.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,选项C为易错点,注意题中无色溶液的体积.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
某KCl、MgCl2、Mg(NO3)2形成的混合中,c(K+)=0.20mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.20mol/L,则c(NO3-)为( )
| A、0.15mol/L |
| B、0.10mol/L |
| C、0.25mol/L |
| D、0.50mol/L |
在有机物分子中能够引入羟基的反应有( )
①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤还原反应 ⑥加聚反应.
①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤还原反应 ⑥加聚反应.
| A、①②③④ | B、②③④⑤ |
| C、①②④⑤ | D、①②⑤⑥ |
最近研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
A、羰基硫的电子式为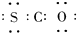 |
| B、羰基硫分子的中心原子为氧 |
| C、羰基硫中三个原子处于同一直线上 |
| D、羰基硫是非极性分子 |
某温度下,将Cl2通入KOH溶液中得KCl、KClO3和KClO的混合溶液.经测定ClO3-和ClO-物质的量之比为2:1,则反应中被还原的Cl2与被氧化Cl2的物质的量之比为( )
| A、2:3 | B、3:4 |
| C、11:3 | D、10:3 |
下列溶液的导电能力变化最大(忽略溶液体积变化)的是( )
| A、向100mL含有0.05 molHCI的溶液中加入等物质的量的NaOH固体 |
| B、向100mL含有0.05 molCH3COOH的溶液中通入等物质的量的氨气 |
| C、向100mL含有0.05 molHCI的溶液中加入等物质的量的NaHCO3固体 |
| D、向100mL含有0.05 molCa(OH)2的澄清石灰水中通入标况下224mLCO2气体 |
下列说法正确的是( )
| A、84消毒液的有效成分为次氯酸钠,起消毒作用的成分为次氯酸 |
| B、漂白粉的有效成分为次氯酸钙,是纯净物 |
| C、ClO2也可用于漂白消毒,消毒能力比氯气弱 |
| D、干燥的氯气不能使鲜花褪色 |
下列说法正确的是( )
| A、通式相同的不同物质一定属于同系物 |
| B、在相同条件下,燃烧等物质的量的C2H4和C2H5OH,消耗的O2体积相等 |
| C、相对分子质量相同的不同物质一定是同分异构体 |
| D、分子内有苯环和羟基的化合物一定是酚类 |