题目内容
NA为阿伏加德罗常数,下述正确的是( )
| A、80g硝酸铵(NH4NO3)含有氮原子数为2NA |
| B、1L1mol?L-1的盐酸溶液中,所含氯化氢分子数为NA |
| C、标准状况下,11.2L酒精(C2H5OH)所含分子数为0.5NA |
| D、在钠与氯气的反应中,1mol钠失去的电子数为2 NA |
考点:阿伏加德罗常数
专题:
分析:A、依据n=
计算物质的量,结合化学式计算氮原子数;
B、盐酸溶液中氯化氢全部电离,溶液中无氯化氢分子;
C、酒精在标准状况不是气体;
D、1mol钠失去1mol电子,据此分析.
| m |
| M |
B、盐酸溶液中氯化氢全部电离,溶液中无氯化氢分子;
C、酒精在标准状况不是气体;
D、1mol钠失去1mol电子,据此分析.
解答:
解:A、80克NH4NO3物质的量=
1mol;含氮原子数为2NA,故A正确;
B、盐酸溶液中氯化氢全部电离,溶液中无氯化氢分子,故B错误;
C、酒精在标准状况不是气体,11.2L酒精物质的量不是0.5mol,故C错误;
D、1mol钠只能失去1mol电子,故D错误,
故选A.
| 80g |
| 80g/mol |
B、盐酸溶液中氯化氢全部电离,溶液中无氯化氢分子,故B错误;
C、酒精在标准状况不是气体,11.2L酒精物质的量不是0.5mol,故C错误;
D、1mol钠只能失去1mol电子,故D错误,
故选A.
点评:本题考查了阿伏加德罗常数的应用,主要是质量换算物质的量计算微粒数,气体摩尔体积的条件应用,题目较简单.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列物质中,不能发生消去反应的是( )
A、 |
| B、CH3 CH2Br |
C、 |
| D、CH2ClCH2CH3 |
在甲酸的下列性质中,可以证明它是弱电解质的是( )
| A、1mol/L甲酸溶液中c(H+)约为1×10-2mol/L |
| B、甲酸能与水以任意比互溶 |
| C、10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应 |
| D、甲酸的导电性比强酸溶液的导电性弱 |
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol,
②稀溶液中,H+(aq)+OH-(aq)=H2O;△H=-57.3kJ/mol下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O;△H=-57.3kJ/mol下列结论正确的是( )
| A、碳的燃烧热大于110.5 kJ/mol |
| B、①的反应热为221 kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为114.6 kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、Na2S |
| B、Cl2 |
| C、NaHCO3 |
| D、CO2 |
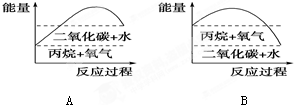
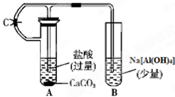 根据如图所示装置,请回答:
根据如图所示装置,请回答: