题目内容
实验需要0.1mol/LNaOH溶液450ml,根据溶液配制中情况回答下列问题:
(1)实验中除了托盘天平、烧杯、量筒、胶头滴管外还需要的其它仪器有:
(2)根据计算得知,所需NaOH的质量为 g
(3)下列操作对所配浓度有何影响(填写字母)偏大的有 ;偏小的有 ;无影响的有 .
A、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
B、往容量瓶转移时,有少量液体溅出
C、未洗涤溶解NaOH的烧杯
D、定容时仰视刻度线
E、容量瓶未干燥即用来配制溶液
H、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
(1)实验中除了托盘天平、烧杯、量筒、胶头滴管外还需要的其它仪器有:
(2)根据计算得知,所需NaOH的质量为
(3)下列操作对所配浓度有何影响(填写字母)偏大的有
A、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
B、往容量瓶转移时,有少量液体溅出
C、未洗涤溶解NaOH的烧杯
D、定容时仰视刻度线
E、容量瓶未干燥即用来配制溶液
H、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据配制溶液的实验操作过程选择所用仪器.
(2)根据n=cv计算氢氧化钠的物质的量,再根据m=nM计算所需氢氧化钠的质量.
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
分析判断.
(2)根据n=cv计算氢氧化钠的物质的量,再根据m=nM计算所需氢氧化钠的质量.
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
| n |
| V |
解答:
解:(1)没有450mL规格容量瓶,所以选用500mL容量瓶.
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙.
根据提供的仪器可知,还需仪器有玻璃棒、500ml容量瓶.
故答案为:玻璃棒、500ml容量瓶.
(2)需氢氧化钠的质量为m=0.5L×0.1mol?L-1×40g/mol=2.0g.
故答案为:2.0g.
(3)A.液体具有热胀冷缩的性质,氢氧化钠溶解放热,未冷却到室温,趁热将溶液到入容量瓶,并配成溶液,会导致溶液体积偏小,溶液浓度偏高;
B.往容量瓶转移时,有少量液体溅出,移入容量瓶中的氢氧化钠的质量减小,所配溶液浓度偏低;
C.未洗涤烧杯、玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低
D.定容时,仰视刻度线,导致溶液体积增大,所配溶液浓度偏低;
E.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响.
H.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
故偏大的有A,偏低的有BCDH,无影响的有E.
故答案为:A;B C D H;E.
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙.
根据提供的仪器可知,还需仪器有玻璃棒、500ml容量瓶.
故答案为:玻璃棒、500ml容量瓶.
(2)需氢氧化钠的质量为m=0.5L×0.1mol?L-1×40g/mol=2.0g.
故答案为:2.0g.
(3)A.液体具有热胀冷缩的性质,氢氧化钠溶解放热,未冷却到室温,趁热将溶液到入容量瓶,并配成溶液,会导致溶液体积偏小,溶液浓度偏高;
B.往容量瓶转移时,有少量液体溅出,移入容量瓶中的氢氧化钠的质量减小,所配溶液浓度偏低;
C.未洗涤烧杯、玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低
D.定容时,仰视刻度线,导致溶液体积增大,所配溶液浓度偏低;
E.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响.
H.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
故偏大的有A,偏低的有BCDH,无影响的有E.
故答案为:A;B C D H;E.
点评:本题考查了一定物质的量浓度溶液的配制,注意从c=
理解配制原理.
| n |
| V |

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
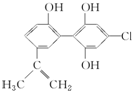 禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )
禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )| A、1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH |
| B、1 mol X与足量浓溴水反应,最多消耗4 mol Br2 |
| C、X遇FeCl3溶液显色,可看作酚类物质 |
| D、兴奋剂X所有碳原子有可能共平面 |