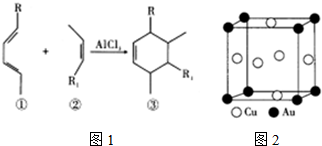
题目内容
4.COCl2(g)?CO(g)+Cl2(g)△H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是( )| A. | 恒容通入惰性气体 | B. | 恒压时通入惰性气体 | ||
| C. | 恒容通入COCl2气体 | D. | 加催化剂 |
分析 该反应为气体体积增大且吸热的反应,则提高COCl2转化率,可减小压强或升高温度使平衡正向移动,以此来解答.
解答 解:A.恒容通入惰性气体,反应体系中各物质的浓度不变,反应速率不变,平衡不移动,转化率不变,故A不选;
B.恒压时通入惰性气体,反应体系的压强减小,则平衡正向移动,转化率增大,故B选;
C.恒容通入COCl2气体,压强增大,平衡逆向移动,转化率减小,故C不选;
D.加催化剂,平衡不移动,转化率不变,故D不选;
故选B.
点评 本题考查化学平衡的影响因素,为高频考点,把握浓度、压强对化学平衡的影响为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.离子键和共价键可能同时存在于同一化合物中.下列化合物中既存在离子键又存在共价键的是( )
| A. | KBr | B. | Na2O | C. | HBr | D. | NH4NO3 |
14.Cu2O和CuO组成的混合物中,Cu的质量分数为88%,则混合物中含Cu2O和CuO的物质的量之比( )
| A. | 5:1 | B. | 4:1 | C. | 3:2 | D. | 1:5 |
19.已知:4P(红磷,S)═P4(白磷,s)△H=+17kJ•moL-1,则下列推论正确的是( )
| A. | 当1 mol白磷完全转变成红磷时放出17kJ热量 | |
| B. | 正反应是一个放热反应 | |
| C. | 当4g红磷转变成白磷时吸收I7k J热量 | |
| D. | 白磷比红磷稳定 |
9.有下列八种物质:①氯化钙、②金刚石、③硫、④氢氧化钠、⑤二氧化硅、⑥干冰,回答有关这八种物质的问题.(用编号回答)
(1)将这八种物质按不同晶体类型分成四组,并填写下表:
(2)属于共价化合物的是⑤⑥;含有共价键的离子化合物是④;
(3)其中硬度最大的物质是②;熔点最低的物质是⑥.
(1)将这八种物质按不同晶体类型分成四组,并填写下表:
| 晶体类型 | 离子晶体 | 原子晶体 | 分子晶体 |
| 各组中物质的编号 | ①④ | ②⑤ | ③⑥ |
(3)其中硬度最大的物质是②;熔点最低的物质是⑥.
14.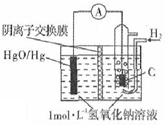 某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )
某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )
 某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )
某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )| A. | 正极反应为:HgO(s)-2e-+H20=Hg(l)+2OH- | |
| B. | 放电结束后,溶液中的pH值下降 | |
| C. | 每反应2.24L氢气,交换膜通过0.2mol离子 | |
| D. | 电子通过离子交换膜从负极向正极移动,保持溶液中电荷平衡 |