题目内容
下列装置或操作能达到目的是( )
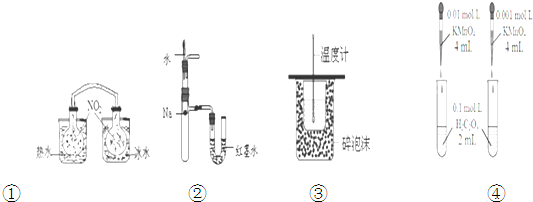

| A、装置①依据两容器内气体颜色变化,不能判断反应2NO2(g)?N2O4(g)平衡移动的方向 |
| B、装置②依据U管两边液面的高低判断Na和水反应的热效应 |
| C、装置③测定中和热 |
| D、装置④依据褪色快慢比较浓度对反应速率的影响 |
考点:化学实验方案的评价
专题:
分析:A.N2O4是红棕色气体,放入热水中,平衡逆向移动,放入冷水中平衡正向移动;
B.钠与反应放热,大试管内气体受热膨胀;
C.缺少搅拌器;
D.浓度不同其它条件相同时,根据溶液褪色快慢确定浓度对化学反应速率的影响.
B.钠与反应放热,大试管内气体受热膨胀;
C.缺少搅拌器;
D.浓度不同其它条件相同时,根据溶液褪色快慢确定浓度对化学反应速率的影响.
解答:
解:A.反应2NO2(g)?N2O4(g)为放热反应,放入热水中,平衡逆向移动,二氧化氮的浓度增大,颜色加深;放入冷水中,平衡正向移动,二氧化氮浓度减小,颜色变浅,所以能实现实验目的,故A错误;
B.钠与反应放热,大试管内气体受热膨胀,U管左侧液面下降,右侧液面上升,所以能实现实验目的,故B正确;
C.装置③测定中和热,缺少搅拌器,导致测量不准确,故C错误;
D.两种溶液中高锰酸钾溶液浓度不同,其它条件相同,所以可以根据溶液褪色时间判断浓度对反应速率的影响,故D正确.
故选BD.
B.钠与反应放热,大试管内气体受热膨胀,U管左侧液面下降,右侧液面上升,所以能实现实验目的,故B正确;
C.装置③测定中和热,缺少搅拌器,导致测量不准确,故C错误;
D.两种溶液中高锰酸钾溶液浓度不同,其它条件相同,所以可以根据溶液褪色时间判断浓度对反应速率的影响,故D正确.
故选BD.
点评:本题考查化学实验方案评价,侧重考查基本操作、基本原理,明确实验原理是解本题关键,注意从装置的目的性、操作的准确性等方面评价,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
将Fe(OH)3露置在空气中加热灼烧所得的产物为( )
| A、FeO |
| B、Fe2O3 |
| C、Fe3O4 |
| D、Fe(OH)3 |
铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL NO2气体和224mL的NO气体(气体的体积已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
| A、7.04 g |
| B、8.26 g |
| C、8.51 g |
| D、9.02 g |
 I.某校化学学习小组为了探究草酸(H2C2O4)的化学性质,设计了如下实验:
I.某校化学学习小组为了探究草酸(H2C2O4)的化学性质,设计了如下实验: 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.


