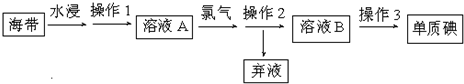
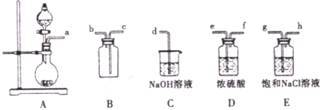
��Ŀ����
�ס��ҡ�������Ϊǰ������Ԫ���γɵ��������ǵĵ���������Ϊ14����֪��Ϊԭ�ӣ��ҡ�������Ϊ˫ԭ�ӷ��ӻ����ӣ�
��1����ԭ�ӽṹʾ��ͼ�� ��
��2������˫ԭ�ӷ��ӣ��ڸ���ʱ��һ�ֻ�ԭ����14g��ȼ�շų���������141.5kJ��д����ȼ�յ��Ȼ�ѧ����ʽ ��
��3����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬��д���ÿ�ȼ������������1��1�ӳɺ�IJ�����Ӿ۷�Ӧ�ķ���ʽ ��
��4���ɶ�������ɵ��������ڵ��ʣ���ɶ���Ԫ�ص�����������Ӧ��ˮ����X����ͼ��ʾת����ϵ����Ӧ�����������������ԣ���
����֪WΪ�����������ʣ�W�����ڱ��е�λ�� ��д��X��ϡ��Һ��Z��Ӧ�����ӷ���ʽ ��
��X��Ũ��Һ��W�ڼ��������·�Ӧ��������Q����֪Q���ȷ�������ķֽⷴӦ��1mol Q�ֽ�ʱ����2mol����ת�ƣ�Q�����ֽⷴӦ�Ļ�ѧ����ʽ�� ����Qװ���ܱ������У����ȵ�T�棬��ƽ��ʱ������ܱ�����������ѹǿ�Ƿ�Ӧ��ʼʱ��1.25����Q�ķֽ���Ϊ ��
��1����ԭ�ӽṹʾ��ͼ��
��2������˫ԭ�ӷ��ӣ��ڸ���ʱ��һ�ֻ�ԭ����14g��ȼ�շų���������141.5kJ��д����ȼ�յ��Ȼ�ѧ����ʽ
��3����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬��д���ÿ�ȼ������������1��1�ӳɺ�IJ�����Ӿ۷�Ӧ�ķ���ʽ
��4���ɶ�������ɵ��������ڵ��ʣ���ɶ���Ԫ�ص�����������Ӧ��ˮ����X����ͼ��ʾת����ϵ����Ӧ�����������������ԣ���

����֪WΪ�����������ʣ�W�����ڱ��е�λ��
��X��Ũ��Һ��W�ڼ��������·�Ӧ��������Q����֪Q���ȷ�������ķֽⷴӦ��1mol Q�ֽ�ʱ����2mol����ת�ƣ�Q�����ֽⷴӦ�Ļ�ѧ����ʽ��
���㣺������ƶ�
ר�⣺�ƶ���
��������Ϊԭ�ӣ��������Ϊ14��ӦΪSiԪ�أ��ҡ�������Ϊ˫ԭ�ӷ��ӻ����ӣ�����������Ϊ14��������CO��N2��C22-�ȣ�����˫ԭ�ӷ��ӣ��ڸ���ʱ��һ�ֻ�ԭ����ӦΪCO����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬������Ϊ��Ȳ�����ΪC22-��
��������ɵ��������ڵ��ʣ�ӦΪN2����Ӧ������������ˮ����ΪHNO3����ת����ϵ��֪WΪ��۽�����ӦΪFe����YΪFe��NO3��3��ZΪFe��NO3��2���Դ˽����⣮
��������ɵ��������ڵ��ʣ�ӦΪN2����Ӧ������������ˮ����ΪHNO3����ת����ϵ��֪WΪ��۽�����ӦΪFe����YΪFe��NO3��3��ZΪFe��NO3��2���Դ˽����⣮
���
�⣺��Ϊԭ�ӣ��������Ϊ14��ӦΪSiԪ�أ��ҡ�������Ϊ˫ԭ�ӷ��ӻ����ӣ�����������Ϊ14��������CO��N2��C22-�ȣ�����˫ԭ�ӷ��ӣ��ڸ���ʱ��һ�ֻ�ԭ����ӦΪCO����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬������Ϊ��Ȳ�����ΪC22-��
��������ɵ��������ڵ��ʣ�ӦΪN2����Ӧ������������ˮ����ΪHNO3����ת����ϵ��֪WΪ��۽�����ӦΪFe����YΪFe��NO3��3��ZΪFe��NO3��2��
��1����ΪSi��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ4��ԭ�ӽṹʾ��ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��14g COȼ�շų���������141.5kJ����0.5mol COȼ�գ���2molCOȼ�շų�������Ϊ566kJ���Ȼ�ѧ����ʽΪ2CO��g��+O2��g��=2CO2��g������H=-566kJ?mol-1���ʴ�Ϊ��2CO��g��+O2��g��=2CO2��g����H=-566kJ?mol-1��
��3����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬������Ϊ��Ȳ��������1��1�ӳɺ�IJ���ΪCH2=CH2�������Ӿ۷�Ӧ�Ļ�ѧ����ʽΪnCH2=CH2
 ��
��
�ʴ�Ϊ��nCH2=CH2
 ��
��
��4���������Ϸ�����֪WΪFe��λ�����ڱ��������ڵڢ����壬X��ϡ��Һ��Z��Ӧ�����ӷ���ʽΪ3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
�ʴ�Ϊ���������ڵڢ����壻3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��X��Ũ��Һ��W�ڼ��������·�Ӧ��������Q��ӦΪNO2����֪NO2���ȷ�������ķֽⷴӦ��1mol NO2�ֽ�ʱ����2mol����ת�ƣ�˵��NԪ�ػ��ϼ۱仯2�ۣ�Ӧ����NO������ʽΪ2NO2
2NO+O2����Qװ���ܱ������У����ȵ�T�棬��ƽ��ʱ������ܱ�����������ѹǿ�Ƿ�Ӧ��ʼʱ��1.25���������ʵ���Ϊ��ʼʱ��1.25����
��ԭ��1molNO2��ת��xmol����
2NO2
2NO+O2
x x 0.5x
=1.25��
x=0.5��ת����Ϊ
��100%=50%��
�ʴ�Ϊ��2NO2
2NO+O2��50%��
��������ɵ��������ڵ��ʣ�ӦΪN2����Ӧ������������ˮ����ΪHNO3����ת����ϵ��֪WΪ��۽�����ӦΪFe����YΪFe��NO3��3��ZΪFe��NO3��2��
��1����ΪSi��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ4��ԭ�ӽṹʾ��ͼΪ
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����2��14g COȼ�շų���������141.5kJ����0.5mol COȼ�գ���2molCOȼ�շų�������Ϊ566kJ���Ȼ�ѧ����ʽΪ2CO��g��+O2��g��=2CO2��g������H=-566kJ?mol-1���ʴ�Ϊ��2CO��g��+O2��g��=2CO2��g����H=-566kJ?mol-1��
��3����Ϊ˫ԭ�Ӷ��������ӣ����������ɵĻ������ܸ�ˮ��Ӧ����һ�ֿ�ȼ�����壬������Ϊ��Ȳ��������1��1�ӳɺ�IJ���ΪCH2=CH2�������Ӿ۷�Ӧ�Ļ�ѧ����ʽΪnCH2=CH2
| ���� |
 ��
���ʴ�Ϊ��nCH2=CH2
| ���� |
 ��
����4���������Ϸ�����֪WΪFe��λ�����ڱ��������ڵڢ����壬X��ϡ��Һ��Z��Ӧ�����ӷ���ʽΪ3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
�ʴ�Ϊ���������ڵڢ����壻3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��X��Ũ��Һ��W�ڼ��������·�Ӧ��������Q��ӦΪNO2����֪NO2���ȷ�������ķֽⷴӦ��1mol NO2�ֽ�ʱ����2mol����ת�ƣ�˵��NԪ�ػ��ϼ۱仯2�ۣ�Ӧ����NO������ʽΪ2NO2
| �� |
��ԭ��1molNO2��ת��xmol����
2NO2
| �� |
x x 0.5x
| 1-x+x+0.5x |
| 1 |
x=0.5��ת����Ϊ
| 0.5 |
| 1 |
�ʴ�Ϊ��2NO2
| �� |
���������⿼��λ�ýṹ���ʵ����ϵ��Ӧ���Լ����ƶ��⣬��Ŀ��Ϊ�ۺϣ���Ŀ�ѶȽϴ�ע����ȷ�ƶ�Ԫ�ص����࣬ȷ�����йػ���֪ʶΪ������Ĺؼ���

��ϰ��ϵ�д�
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
�����Ŀ
��֪H-H�����ܣ�����ʱ���ջ�����ʱ�ͷŵ�������Ϊ436kJ?mol-1��N-H������Ϊ391kJ?mol-1�������Ȼ�ѧ����ʽ��N2��g��+3H2��g���T2NH3��g����H=-92.4kJ?mol-1����N��N���ļ����ǣ�������
| A��431kJ?mol-1 |
| B��896kJ?mol-1 |
| C��649kJ?mol-1 |
| D��945.6kJ?mol-1 |
�Ҵ���������ˮ�ķ�Ӧ���ڣ�������
| A���Ӿ۷�Ӧ | B��ȡ����Ӧ |
| C���ӳɷ�Ӧ | D����ȥ��Ӧ |