题目内容
某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2 mol该离子恰好能使0.6molSO32-离子完全氧化,则X2O72-离子还原后的化合价为
A.+1 B.+2 C.+3 D.+4
C
【解析】
试题分析:在氧化还原反应中得失电子数目相等。在X2O72-中X的化合价是+6价,假设反应后元素的化合价是+m价,由于SO32-离子反应后元素的化合价变为+6价,所以0.2×2×(6-m)=0.6×(6-4),解得m=+3价,因此选项是C。
考点:考查氧化还原反应中化合价升降总数相等在确定物质中元素的化合价的应用的知识。

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
 2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性
2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性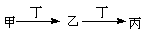 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是