题目内容
下列推论正确的是
A.在粗硅的制取中发生反应2C+SiO2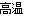 2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性
2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性
B.由“HF比HCl稳定性好”,可推知HF比HCl沸点高
C.由“同温度下等浓度的Na2CO3溶液比Na2SO4溶液的pH大”,可推知C比S的非金属性弱
D.由“某过程发生化学键断裂”,可推知该过程发生了化学变化
C
【解析】
试题分析:A.非金属元素的单质的氧化性越强,则非金属性越强,在粗硅的制取中发生反应2C+SiO2 2CO↑+Si,C作还原剂,不能根据高温下非自发反应比较非金属性,所以不能推知碳的非金属性强于硅的非金属性,故A错误;B.稳定性与化学键有关,H-F键能大,则HF稳定,而HF中含氢键,所以HF沸点比HCl高,沸点与稳定性没有因果关系,故B错误;C.等浓度的Na2CO3溶液比Na2SO4溶液的pH大,则碳酸的酸性小于硫酸,最高价氧化物的水化物的酸性越强,非金属性越强,故C正确;D.某过程发生化学键断裂,不一定发生化学变化,如HCl溶于水,没有化学键生成,故D错误;故选C。
2CO↑+Si,C作还原剂,不能根据高温下非自发反应比较非金属性,所以不能推知碳的非金属性强于硅的非金属性,故A错误;B.稳定性与化学键有关,H-F键能大,则HF稳定,而HF中含氢键,所以HF沸点比HCl高,沸点与稳定性没有因果关系,故B错误;C.等浓度的Na2CO3溶液比Na2SO4溶液的pH大,则碳酸的酸性小于硫酸,最高价氧化物的水化物的酸性越强,非金属性越强,故C正确;D.某过程发生化学键断裂,不一定发生化学变化,如HCl溶于水,没有化学键生成,故D错误;故选C。
考点:考查稳定性、氢键、非金属性比较、化学键与化学反应的关系等

练习册系列答案
相关题目

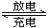 LixV2O5。下列说法中正确的是
LixV2O5。下列说法中正确的是 CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,下列说法正确的是
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,下列说法正确的是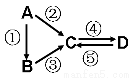
 常用于测定动植物标本的年龄.关于
常用于测定动植物标本的年龄.关于