题目内容
有200mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)=0.2 mol/L,c(Cl-)=1.3 mol/L,要使Mg2+全部转化为沉淀分离出来,至少需要4mol/L NaOH 溶液的体积是
A. 40mL B.72 mL C. 80 mL D.128mL
C
【解析】
试题分析:根据电荷守恒可得3c(Al3+)+2 c(Mg2+)= c(Cl-). c(Al3+)=(1.3-2×0.2)÷3=0.3mol/L.所以要想使Mg2+全部转化为沉淀分离出来,则Mg2+应该变为Mg(OH)2沉淀,而Al3+转化为AlO2-. n(Al3+)=0.3mol/L ×02L=0.06mol,根据方程式Al3++4OH-= AlO2-+ 2H2O可知消耗NaOH的物质的量是0.24mol;n(Mg2+)= 0.2 mol/L ×0.2L=0.04mol, 根据方程式Mg2++2OH-= Mg(OH)2↓可知其消耗NaOH的物质的量是0.08 mol;所以一共消耗的NaOH的物质的量是0.24mol+0.08mol=0.32mol,则至少需要4mol/L NaOH 溶液的体积是V=n÷C=0.32mol÷4mol/L=0.08L=80ml,因此选项是C。
考点:考查元素集化合物的性质及电荷守恒在化学计算中的应用的知识。

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
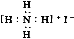

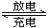 LixV2O5。下列说法中正确的是
LixV2O5。下列说法中正确的是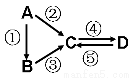
 CO2+H2 B.3NO2+H2O===2HNO3+NO
CO2+H2 B.3NO2+H2O===2HNO3+NO KClO3 + 5KCl + 3H2O反应,以下说法错误的是
KClO3 + 5KCl + 3H2O反应,以下说法错误的是