题目内容
16.常温下,在溶液中可以发生反应:X+2Y3+═2Y2++X2+,对下列叙述的判断正确的是( )①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物 ⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强.
| A. | ②③④⑥ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ①②⑤⑥ |
分析 由X+2Y3+=2Y2++X2+可知,X的化合价升高,Y的化合价降低,则X作还原剂,具有还原性,被氧化,发生氧化反应;Y3+具有氧化性,结合氧化剂的氧化性大于氧化产物的氧化性来解答.
解答 解:由X+2Y3+=2Y2++X2+可知,X的化合价升高,Y的化合价降低,
①X作还原剂,被氧化,故①正确;
②X的化合价升高,X是还原剂,故②错误;
③X是还原剂,具有还原性,故③正确;
④Y的化合价降低,Y2+是还原产物,故④错误;
⑤Y2+的化合价能升高,则具有还原性,故⑤正确;
⑥由氧化剂的氧化性大于氧化产物的氧化性,则Y3+的氧化性比X2+的氧化性强,故⑥正确;
故选C.
点评 本题考查氧化还原反应,明确元素的化合价是解答本题的关键,并熟悉氧化还原反应中的概念来解答,难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
7.下列说法正确的是( )
| A. | 一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应 | |
| B. | C3H6与C4H8一定互为同系物 | |
| C. | 全降解塑料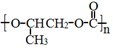 可由环氧丙烷 可由环氧丙烷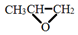 和CO2缩聚制得 和CO2缩聚制得 | |
| D. | 一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,生成水的质量为18(1-a)g |
4.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下NA个SO3的体积为22.4 L | |
| B. | 1 mol Fe与足量的HCl反应,转移的电子数为3NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
11.下列实验操作中,错误的是( )
| A. | 倾倒液体时试剂瓶标签面向手心. | |
| B. | 玻璃棒蘸取溶液滴到放在表面皿上湿润的pH试纸上. | |
| C. | 用HCl溶液洗涤并灼烧铂丝后,再进行焰色反应. | |
| D. | KOH溶液保存在带磨口玻璃塞的试剂瓶中. |
1.下列化合物中,既能发生消去反应,又能发生水解反应的是( )
| A. | 三氯甲烷 | B. | 2-丙醇 | C. | 2-氯丙烷 | D. | 乙酸乙酯 |
5. 在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
 在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )| A. | lg$\frac{{V}_{2}}{{V}_{1}}$=6时,HA溶液的pH=8 | |
| B. | pH相同时,c(HA)>c(HB) | |
| C. | 曲线上a、b两点 $\frac{[{B}^{-}]}{[HB][O{H}^{-}]}$ 一定不相等 | |
| D. | 25℃时,NaA溶液的pH一定小于NaB溶液 |
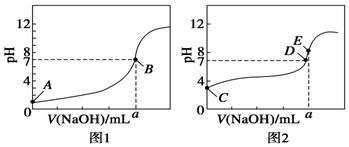 常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.
常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.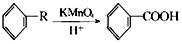 从A出发,发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体.
从A出发,发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体.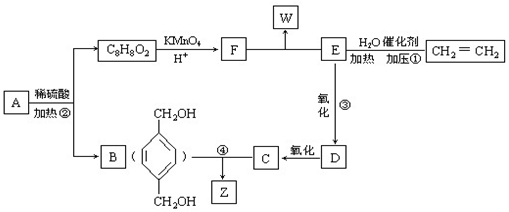
 +2CH3COOH$?_{△}^{浓硫酸}$
+2CH3COOH$?_{△}^{浓硫酸}$ +2H2O.
+2H2O.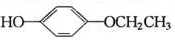 、
、 、
、 、
、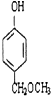 任意2个 (任写两种)
任意2个 (任写两种)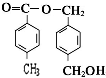 .
.