题目内容
7.下列说法正确的是( )| A. | 一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应 | |
| B. | C3H6与C4H8一定互为同系物 | |
| C. | 全降解塑料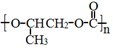 可由环氧丙烷 可由环氧丙烷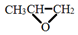 和CO2缩聚制得 和CO2缩聚制得 | |
| D. | 一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,生成水的质量为18(1-a)g |
分析 A.葡萄糖为单糖,不能水解;
B.C3H6与C4H8可能为烯烃或环烷烃;
C.由结构简式可知全降解塑料(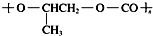 )可由单体环氧丙烷(
)可由单体环氧丙烷(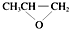 )和CO2加聚制得;
)和CO2加聚制得;
D.乙烯的分子式为C2H4,甲醛的分子式为CH2O,两物质中C、H原子数目之比都是1:2,故混合物中C、H元素质量之比=12:2=6:1,根据氧元素质量分数计算C、H元素质量分数之和,进而计算氢元素质量分数.
解答 解:A.葡萄糖为单糖,不能发生水解,乙酸乙酯、蛋白质都能与水发生水解反应,故A错误;
B.C3H6与C4H8可能为烯烃或环烷烃,不一定为同系物,故B错误;
C.由结构简式可知全降解塑料(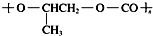 )可由单体环氧丙烷(
)可由单体环氧丙烷(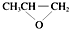 )和CO2加聚制得,不是缩聚反应,故C错误;
)和CO2加聚制得,不是缩聚反应,故C错误;
D.乙烯的分子式为C2H4,甲醛的分子式为CH2O,两物质中C、H原子数目之比都是1:2,故混合物中C、H元素质量之比=12:2=6:1,含氧的质量分数为a,则C、H元素质量分数之和为1-a,故H元素质量分数=(1-a)×$\frac{1}{1+6}$=$\frac{1-a}{7}$,生成水的质量为14g×$\frac{1-a}{7}$×$\frac{1}{2}$×18=18(1-a)g,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.在同温同压下,有同质量的气体甲与乙,已知此时甲的体积小于乙的体积.则下列说法正确的是( )
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的摩尔体积比乙的摩尔体积小 | |
| C. | 甲的相对分子质量比乙的相对分子质量大 | |
| D. | 甲的物质的量比乙的物质的量少 |
2.在一恒温、恒容的密闭容器中发生反应A(s)+2B(g)?C(g)+D(g),当下列物理量不再变化时,能够表明该反应已达平衡状态的是( )
| A. | 混合气体的压强 | B. | D的物质的量浓度 | ||
| C. | A的物质的量浓度 | D. | 气体的总物质的量 |
19.NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,44.8 LH2O含有的水分子数为2NA | |
| B. | 88gC02含有的C02分子数为2NA | |
| C. | 46gNO2气体含有的氧原子数为NA | |
| D. | 1mol的任何气体中都含有NA个原子 |
16.常温下,在溶液中可以发生反应:X+2Y3+═2Y2++X2+,对下列叙述的判断正确的是( )
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物 ⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强.
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物 ⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强.
| A. | ②③④⑥ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ①②⑤⑥ |
17.实验室中需要配制2mol/L的NaCl溶液480mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A. | 480mL 56.2g | B. | 500mL 58.5g | ||
| C. | 1000mL 58.5g | D. | 任意规格 56.2g |