题目内容
下列反应属于放热反应的是( )
| A、焦炭和二氧化碳共热 |
| B、NaOH溶于水 |
| C、KClO3受热分解 |
| D、CaO溶于水 |
考点:吸热反应和放热反应
专题:
分析:常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应、所有中和反应、绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、少数分解、置换以及某些复分解反应(如铵盐和强碱).
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、少数分解、置换以及某些复分解反应(如铵盐和强碱).
解答:
解:A.焦炭和二氧化碳共热属于吸热反应,故A错误;
B.NaOH溶于水,有热量放出,是物理变化,不属于放热反应,故B错误;
C.KClO3受热分解属于吸热反应,故C错误;
D.CaO溶于水属于放热反应,故D正确.
故选D.
B.NaOH溶于水,有热量放出,是物理变化,不属于放热反应,故B错误;
C.KClO3受热分解属于吸热反应,故C错误;
D.CaO溶于水属于放热反应,故D正确.
故选D.
点评:本题考查放热反应,难度不大.抓住中学化学中常见的吸热或放热的反应是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列事实,可以用盐的水解反应解释的是( )
①泡沫灭火器内盛饱和碳酸氢钠溶液和硫酸铝浓溶液
②配制硝酸银溶液时,需加少量硝酸防止溶液浑浊
③生活中可用热的纯碱溶液清洗餐具上的油污
④KA1(SO4)2.12H2O可用于沉淀水中的不溶物
⑤可以用食醋除去热水瓶里的水垢[成分为CaCO3、Mg(OH)2]
⑥侯德榜联合制碱法的反应原理:NaCl(浓)+NH3+H2O+CO2=NaHCO3↓+NH4Cl.
①泡沫灭火器内盛饱和碳酸氢钠溶液和硫酸铝浓溶液
②配制硝酸银溶液时,需加少量硝酸防止溶液浑浊
③生活中可用热的纯碱溶液清洗餐具上的油污
④KA1(SO4)2.12H2O可用于沉淀水中的不溶物
⑤可以用食醋除去热水瓶里的水垢[成分为CaCO3、Mg(OH)2]
⑥侯德榜联合制碱法的反应原理:NaCl(浓)+NH3+H2O+CO2=NaHCO3↓+NH4Cl.
| A、①②③④⑤⑥ | B、①②③④⑤ |
| C、①②③④ | D、①②④ |
下列反应属于氧化反应的是( )
| A、原电池的正极 |
| B、电解池的阴极 |
| C、燃料电池的燃料 |
| D、电镀池的待镀金属 |
下列电离方程式中,正确的是( )
| A、NaOH═Na++OH- |
| B、2H2O═O2↑+2H2↑ |
| C、H2SO4═H2++SO42- |
| D、Na2CO3═2Na++OH- |
下列溶液中的Cl-浓度与50mL1mol?L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL1mol?L-1 NaCl溶液 |
| B、75mL1mol?L-1CaCl2溶液 |
| C、150mL3mol?L-1 KCl溶液 |
| D、75mL1mol?L-1AlCl3溶液 |
某气态烃0.5mol恰好与1molHCl加成,生成物分子中的氢又可被3molCl2取代,则此气态烃可能是( )
| A、C2H2 |
| B、C2H4 |
| C、CH2=C(CH3)2 |
| D、CH≡C-CH3 |
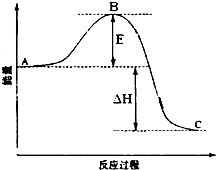 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题: