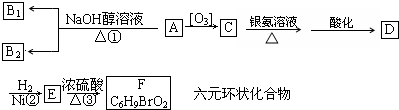
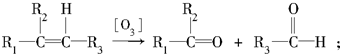
题目内容
写出下列反应的离子方程式:
①用稀硫酸清洗铁锈(Fe2O3)
②NaHCO3溶液与盐酸混合
③向澄清石灰水中通入过量二氧化碳
④向Ba(OH)2溶液中逐滴滴入NaHSO4溶液至Ba2+恰好沉淀完全 .
①用稀硫酸清洗铁锈(Fe2O3)
②NaHCO3溶液与盐酸混合
③向澄清石灰水中通入过量二氧化碳
④向Ba(OH)2溶液中逐滴滴入NaHSO4溶液至Ba2+恰好沉淀完全
考点:离子方程式的书写
专题:
分析:①稀硫酸与三氧化二铁反应生成硫酸铁和水;
②碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水,碳酸氢根离子不能拆开;
③氢氧化钙与过量二氧化碳反应生成碳酸氢钙和水;
④钡离子恰好沉淀,氢氧化钡与硫酸氢钠按照物质的量1:1反应,氢氧根离子过量,离子方程式按照硫酸氢钠的化学式组成书写.
②碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水,碳酸氢根离子不能拆开;
③氢氧化钙与过量二氧化碳反应生成碳酸氢钙和水;
④钡离子恰好沉淀,氢氧化钡与硫酸氢钠按照物质的量1:1反应,氢氧根离子过量,离子方程式按照硫酸氢钠的化学式组成书写.
解答:
解:①稀硫酸与三氧化二铁反应生成硫酸铁和水,反应的离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3+6H+=2Fe3++3H2O;
②碳酸氢钠与盐酸反应生成二氧化碳气体和水,反应的离子方程式为:HCO3-+H+=CO2↑+H2O,
故答案为:HCO3-+H+=CO2↑+H2O;
③氢氧化钙与过量二氧化碳反应生成碳酸氢钙和水,反应的离子方程式为:CO2+OH-=HCO3-,
故答案为:CO2+OH-=HCO3-;
④向Ba(OH)2溶液中逐滴滴入NaHSO4溶液至Ba2+恰好沉淀完全,此时氢氧化钡与硫酸氢钠按照物质的量1:1反应,反应的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O,
故答案为:H++SO42-+Ba2++OH-=BaSO4↓+H2O.
故答案为:Fe2O3+6H+=2Fe3++3H2O;
②碳酸氢钠与盐酸反应生成二氧化碳气体和水,反应的离子方程式为:HCO3-+H+=CO2↑+H2O,
故答案为:HCO3-+H+=CO2↑+H2O;
③氢氧化钙与过量二氧化碳反应生成碳酸氢钙和水,反应的离子方程式为:CO2+OH-=HCO3-,
故答案为:CO2+OH-=HCO3-;
④向Ba(OH)2溶液中逐滴滴入NaHSO4溶液至Ba2+恰好沉淀完全,此时氢氧化钡与硫酸氢钠按照物质的量1:1反应,反应的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O,
故答案为:H++SO42-+Ba2++OH-=BaSO4↓+H2O.
点评:本题考查了离子方程式的书写,题目难度中等,注意掌握常见物质之间反应,明确离子方程式与化学方程式的区别及书写原则,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列两种情况下:①2g CO和2g H2混合②3g CO和1g H2混合,之后在足量氧气中充分燃烧,生成的气体与Na2O2固体(足量)反应,Na2O2固体的质量增加关系为( )
| A、①=② | B、①<② |
| C、①>② | D、无法判断 |
某有机物的结构简式为(如图),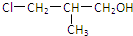 则此有机物可发生的反应类型有( )
则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.
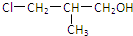 则此有机物可发生的反应类型有( )
则此有机物可发生的反应类型有( )①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.
| A、①②③⑤⑥ |
| B、②③④⑤⑥⑦ |
| C、①③④⑤⑥ |
| D、①②⑤⑥ |
下列物质的保存方法正确的是( )
| A、钠保存在盛有水的试剂瓶中 |
| B、漂白粉露置于空气中 |
| C、浓硝酸保存在棕色玻璃瓶中 |
| D、氢氧化钠溶液保存在带玻璃塞的玻璃瓶中 |
我国合成了一种新的元素A,科学家已经确定它的原子序数是115,请预测A周期表中的位置( )
| A、第7周期第 VA族 |
| B、第6周期第 VB族 |
| C、第7周期第ⅥA族 |
| D、第6周期第 VIIB族 |
地球大气是由多种物质形成的气体混合物,其中含量最高的元素为( )
| A、氮 | B、氦 | C、氢 | D、氧 |
下列反应属于放热反应的是( )
| A、焦炭和二氧化碳共热 |
| B、NaOH溶于水 |
| C、KClO3受热分解 |
| D、CaO溶于水 |