题目内容
已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.
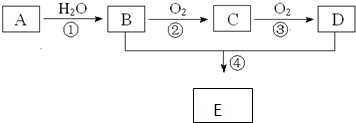
请回答下列问题:
(1)写出A的电子式 ,B、D分子中的官能团名称分别是 、 .
(2)写出下列反应的化学方程式,并注明反应类型:
① ② ④ .

请回答下列问题:
(1)写出A的电子式
(2)写出下列反应的化学方程式,并注明反应类型:
①
考点:有机物的推断
专题:
分析:A的产量通常用来衡量一个国家石油化工水平,则A是乙烯,乙烯和水发生加成反应生成B是乙醇,乙醇和氧气反应生成C,则C是乙醛,C进一步发生氧化反应生成D为乙酸,乙醇与乙酸反应生成E为乙酸乙酯,据此解答.
解答:
解:A的产量通常用来衡量一个国家石油化工水平,则A是乙烯,乙烯和水发生加成反应生成B是乙醇,乙醇和氧气反应生成C,则C是乙醛,C进一步发生氧化反应生成D为乙酸,乙醇与乙酸反应生成E为乙酸乙酯,
(1)A为乙烯,电子式为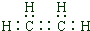 ,B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:
,B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为: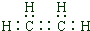 ;羟基;羧基;
;羟基;羧基;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应反应方程式为:CH2=CH2+H2O
CH3CH2OH,
反应②是乙醇发生氧化反应生成乙醛,反应化学方程式为:2 CH3CH2OH+O2
2 CH3CHO+2H2O,
反应④是乙酸与乙醇发生酯化反应生成乙酸乙酯,反应化学方程式为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,也属于取代反应,
故答案为:CH2=CH2+H2O
CH3CH2OH,加成反应;
2 CH3CH2OH+O2
2 CH3CHO+2H2O,氧化反应;
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,酯化反应或取代反应.
(1)A为乙烯,电子式为
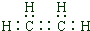 ,B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:
,B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为: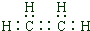 ;羟基;羧基;
;羟基;羧基;(2)反应①是乙烯与水发生加成反应生成乙醇,反应反应方程式为:CH2=CH2+H2O
| 催化剂 |
反应②是乙醇发生氧化反应生成乙醛,反应化学方程式为:2 CH3CH2OH+O2
| Cu |
| △ |
反应④是乙酸与乙醇发生酯化反应生成乙酸乙酯,反应化学方程式为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH2=CH2+H2O
| 催化剂 |
2 CH3CH2OH+O2
| Cu |
| △ |
CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
点评:本题考查有机物的推断,难度不大,根据A的产量是衡量一个国家的石油化工水平判断质为乙烯,再根据反应条件推断,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列方法中,不能用于实验室制备氨气的是( )
| A、加热浓氨水 |
| B、将浓氨水滴到生石灰上 |
| C、加热氯化铵固体 |
| D、将熟石灰和氯化铵的混合物加热 |
下列两种情况下:①2g CO和2g H2混合②3g CO和1g H2混合,之后在足量氧气中充分燃烧,生成的气体与Na2O2固体(足量)反应,Na2O2固体的质量增加关系为( )
| A、①=② | B、①<② |
| C、①>② | D、无法判断 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,11.2 L乙烯含有的极性共价键数为NA |
| B、常温下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.5NA |
| C、16.9 g BaO2固体中阴、阳离子总数为0.2NA |
| D、含有1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
用酒精灯加热时,需要垫石棉网的仪器有( )
①烧杯 ②坩埚 ③锥形瓶 ④蒸发皿 ⑤试管 ⑥烧瓶.
①烧杯 ②坩埚 ③锥形瓶 ④蒸发皿 ⑤试管 ⑥烧瓶.
| A、②④⑤ | B、①②③ |
| C、④⑤⑥ | D、①③⑥ |
某有机物的结构简式为(如图),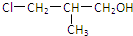 则此有机物可发生的反应类型有( )
则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.
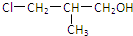 则此有机物可发生的反应类型有( )
则此有机物可发生的反应类型有( )①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.
| A、①②③⑤⑥ |
| B、②③④⑤⑥⑦ |
| C、①③④⑤⑥ |
| D、①②⑤⑥ |
下列物质的保存方法正确的是( )
| A、钠保存在盛有水的试剂瓶中 |
| B、漂白粉露置于空气中 |
| C、浓硝酸保存在棕色玻璃瓶中 |
| D、氢氧化钠溶液保存在带玻璃塞的玻璃瓶中 |
下列反应属于放热反应的是( )
| A、焦炭和二氧化碳共热 |
| B、NaOH溶于水 |
| C、KClO3受热分解 |
| D、CaO溶于水 |