题目内容
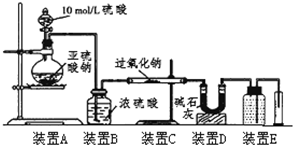 某校化学兴趣小组在学习了过氧化钠性质后,进一步研究其与SO2反应情况,查阅相关资料知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成.有同学认为:CO2、SO2虽然都是酸性氧化物,但SO2具有较强的还原性,CO2无还原性,反应原理应该不相同,并设计如下实验进行探究.
某校化学兴趣小组在学习了过氧化钠性质后,进一步研究其与SO2反应情况,查阅相关资料知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成.有同学认为:CO2、SO2虽然都是酸性氧化物,但SO2具有较强的还原性,CO2无还原性,反应原理应该不相同,并设计如下实验进行探究.(1)[提出假设]向一定量的过氧化钠固体中通入足量的SO2,对反应后的固体产物成分及反应原理提出如下假设:
假设一:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设二:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设三:反应后固体中
(2)[定性研究]
为验证假设三是否成立,兴趣小组进行如下研究,请你完成下表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取反应后的固体放入试管中,… |
①装置D的作用是
②实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据进行判断
| SO2被氧化的程度 | V与m1或m2的关系 |
| 完全被氧化 | V=0 |
| 部分被氧化 | |
| 未被氧化 |
考点:碱金属及其化合物的性质实验
专题:实验设计题
分析:(1)依据假设一和假设二推断假设三为Na2SO3和Na2SO4的混合物,得出结论即可;
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①碱石灰具有碱的性质,可以吸收酸性气体,据此解答;
②若Na2SO3未被氧化发生的反应只有2Na2O2+2SO2=2Na2SO3+O2根据差量法计算即可.
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①碱石灰具有碱的性质,可以吸收酸性气体,据此解答;
②若Na2SO3未被氧化发生的反应只有2Na2O2+2SO2=2Na2SO3+O2根据差量法计算即可.
解答:
解:(1)固体为Na2SO3和Na2SO4的混合物,证明二氧化硫部分被氧化,故答案为:Na2SO3和Na2SO4的混合物;二氧化硫部分被氧化;
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠,故答案为:
;
(3)①碱石灰具有碱的性质,可以吸收酸性气体,故D的作用吸收未反应的SO2,故答案为:吸收未反应的SO2;
②若Na2SO3未被氧化发生的反应只有
2Na2O2+2SO2=2Na2SO3+O2 △m
根据差量法得到V=
或m1=
,若部分被氧化发生的反应还有Na2O2+SO2=Na2SO4,该反应中SO2全部转化为固体的质量,没有气体生成,这个时候固体的质量增大,可知0<V<
;
故答案为:
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠,故答案为:
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸. | 加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解. 证明原固体中既有亚硫酸钠也有硫酸钠. |
(3)①碱石灰具有碱的性质,可以吸收酸性气体,故D的作用吸收未反应的SO2,故答案为:吸收未反应的SO2;
②若Na2SO3未被氧化发生的反应只有
2Na2O2+2SO2=2Na2SO3+O2 △m
根据差量法得到V=
| 7m1 |
| 30 |
| 30V |
| 7 |
| 7m1 |
| 30 |
故答案为:
| SO2被氧化的程度 | V与m1或m2的关系 |
| 完全被氧化 | V=0 |
| 部分被氧化 | 0<V<7m1/30 或m1>30V/7 |
| 未被氧化 | V=7m1/30或m1=30V/7 |
点评:本题以探究实验为基础,探究了过氧化钠和二氧化硫的反应实际情况,考查了化学实验的基本操作、化学实验的设计、装置图分析以及化学反应的计算等有关知识.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
把11g金属混合物加入足量的盐酸中生成5.6LH2(标况),此金属混合物的可能组成为( )
| A、镁、铁 | B、锌、铁 |
| C、铁、铜 | D、镁、钙 |
某温度下,向 2.0L 恒容密闭容器中充入 1.0 molA 和 1.0 molB,发生反应 A(g)+B(g)?C(g)△H<0,经过一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是.
| t/s | 0 | 5 | 10 | 20 | 30 |
| n(A)/moL | 1 | 0.8 | 0.75 | 0.70 | 0.70 |
| A、反应在前 5s 的平均速率v (A)=0.04mol?L-1 |
| B、相同温度下,若平衡后再向容器中充入 0.5 mol A 和 0.5 mol C,反应再次达到平衡前v (正)>v (逆) |
| C、相同温度下,若平衡后移走 0.5 mol A 和 0.5 mol B,反应再次达到平衡时 c(C)小于 0.075 mol?L-1 |
| D、相同温度下,若起始时向容器中充入 2.0 mol C,达到平衡时,C 的转化率大于 70% |
在容积相同的甲、乙两个密闭容器中,分别充入1mol N2、3mol H2,使它们在温度相同的条件下反应,并达到平衡.若甲容器保持体积不变,乙容器保持压强不变,平衡时甲容器中N2的转化率为10%,则乙容器中N2的转化率为( )
| A、10% | B、大于10% |
| C、小于10% | D、5% |
与乙炔具有相同的碳、氢百分含量,但一定既不是它的同系物又不是它的同分异构体的是( )
| A、丙炔 |
| B、乙烯 |
| C、C4H4 |
| D、苯 |
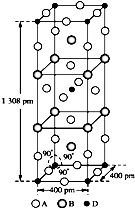 前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题: