��Ŀ����
13��ϡ��Ԫ�ص��������ʺͻ�ѧ���ʼ�Ϊ���ƣ��������ϼ�Ϊ+3�ۣ��ںϽ��м�������ϡ���������ܴ����ƺϽ�����ܣ�����ϡ��Ԫ���ֱ���Ϊұ��ҵ��ά���أ������ƣ�Y��Ԫ���Ǽ���ͳ�������Ҫ���ϣ��ҹ��̲����ŷḻ�ĺ��ƿ�ʯ��Y2FeBe2Si2O10������ҵ��ͨ�������������̿ɻ�������ƣ�
��֪�����йؽ��������γ������������ʱ��pH�����
| ���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
��1��д���ƿ�ʯ���������ƹ���ʱ�Ļ�ѧ����ʽ4Y2FeBe2Si2O10+32NaOH+O2=8Y��OH��3+2Fe2O3+8Na2SiO3+8Na2BeO2+4H2O��
��2������Na2SiO3��Na2BeO2�Ļ����Һ���Ƶ�Be��OH��2��������
�����ѡ�������b�����Լ�����ͨ����Ҫ�IJ�������ʵ�֣�
a��NaOH��Һ b����ˮ c��CO2 d��HNO3
��д��Na2BeO2���������ᷢ����Ӧ�����ӷ���ʽ��BeO22-+4H+=Be2++2H2O��
��3����֪10-2.7=2��10-3��10-3.7=2��10-4����25��ʱ����ӦFe3++3H2O?Fe��OH��3+3H+
��ƽ�ⳣ��K=8��10-5����μ���Fe3+�Ƿ������ȫȡ������Һ���μӼ���KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ�����۲첻��Ѫ��ɫ����˵��Fe3+������ȫ���ش�����������������������������
��4����д�����ɲ����Ƴ����Ļ�ѧ����ʽ2 Y��OH��2��s��+2H2C2O4��aq��=Y2��C2O4��3��s��+6H2O��l����
����H2C2O4��ʪ���KClO3��ϼ��ȵ�60����Ƶù��ʹ��ϵĸ�Ч����������ClO2��д����Ӧ����������������������ʵ���֮��1��1������ˮ��ClO2�ᷢ����Ӧ����Cl2��HClO2��д����Ӧ�Ļ�ѧ����ʽ6ClO2+2H2O=Cl2+4HClO2+3O2��
���� �ƿ�ʯ��Y2FeBe2Si2O10���������������ƹ��ۺ�ˮ�ܹ��˵õ������ơ���������Һ������ΪY��OH��3��Fe2O3������ϡ�����ܽ����백ˮ������ҺPH��3.7��a��6.0��Χ���������ӣ��������백ˮ������ҺPH��8.2���ϼ����������õ������ƣ�����ˮϴ���յõ�Y2O3��
��1���ƿ�ʯ���������ƹ���ʱ��Ӧ���ɹ����ơ���������Һ������ΪY��OH��3��Fe2O3�����ԭ���غ���ƽ��д��
��2�������ڱ��У��롢��Ԫ�ش��ڵڶ����ں͵������ڵĶԽ���λ�ã���ѧ�������ƣ�����Na2SiO3��Na2BeO2�Ļ����Һ���Ƶ�Be��OH��2����������Na2BeO2�����ʺ�NaAlO2����ƶϣ��ӹ��������ᣬ�����Ʒ�Ӧ���ɹ��������Na2BeO2�ķ�Ӧ�����Ȼ�����Һ���ټ��������ˮ���������ӣ�
��Na2BeO2���������ᷴӦ�����Ȼ�����Ȼ�����Һ��
��3����ӦFe3++3H2O?Fe��OH��3+3H+��ƽ�ⳣ��K=$\frac{{c}^{3}��{H}^{+}��}{c��F{e}^{3+}��}$��c��H+��=10-2.7mol/L��ˮ�ⷴӦ�γɵ�����������������Һ��c��Fe3+��=10-5mol/L������������KSCN��Һ�γɺ�ɫ��Һ��
��4�����������ƺͲ��ᷴӦ���ɲ����ƺ�ˮ��
����H2C2O4��ʪ���KClO3��ϼ��ȵ�60����Ƶù��ʹ��ϵĸ�Ч����������ClO2�����ݷ�Ӧ������ϵ������������������������ʵ���֮�ȣ�����ˮ��ClO2�ᷢ����Ӧ����Cl2��HClO2��������ԭ��Ӧ�����غ��жϲ����л�����������
��� �⣺�ƿ�ʯ��Y2FeBe2Si2O10���������������ƹ��ۺ�ˮ�ܹ��˵õ������ơ���������Һ������ΪY��OH��3��Fe2O3������ϡ�����ܽ����백ˮ������ҺPH��3.7��a��6.0��Χ���������ӣ��������백ˮ������ҺPH��8.2���ϼ����������õ������ƣ�����ˮϴ���յõ�Y2O3��
��1���ƿ�ʯ���������ƹ���ʱ��Ӧ���ɹ����ơ���������Һ������ΪY��OH��3��Fe2O3�����ԭ���غ���ƽ��д�õ���ѧ����ʽΪ��4Y2FeBe2Si2O10+32NaOH+O2=8Y��OH��3+2Fe2O3+8Na2SiO3+8Na2BeO2+4H2O��
�ʴ�Ϊ��4Y2FeBe2Si2O10+32NaOH+O2=8Y��OH��3+2Fe2O3+8Na2SiO3+8Na2BeO2+4H2O��
��2�������ڱ��У��롢��Ԫ�ش��ڵڶ����ں͵������ڵĶԽ���λ�ã���ѧ�������ƣ�����Na2SiO3��Na2BeO2�Ļ����Һ���Ƶ�Be��OH��2����������Na2BeO2�����ʺ�NaAlO2����ƶϣ��ӹ��������ᣬ�����Ʒ�Ӧ���ɹ��������Na2BeO2�ķ�Ӧ�����Ȼ�����Һ���ټ��������ˮ���������ӣ�
�ʴ�Ϊ��b��
��Na2BeO2���������ᷢ����Ӧ�����Ȼ����Ȼ��ƺ�ˮ����Ӧ�����ӷ���ʽΪ��BeO22-+4H+=Be2++2H2O��
�ʴ�Ϊ��BeO22-+4H+=Be2++2H2O��
��3����ӦFe3++3H2O?Fe��OH��3+3H+��ƽ�ⳣ��K=$\frac{{c}^{3}��{H}^{+}��}{c��F{e}^{3+}��}$��c��H+��=10-2.7mol/L��ˮ�ⷴӦ�γɵ�����������������Һ��c��Fe3+��=10-5mol/L����ƽ�ⳣ��K=$\frac{{c}^{3}��{H}^{+}��}{c��F{e}^{3+}��}$=$\frac{��1{0}^{-2.7}��^{3}}{1{0}^{-5}}$=8��10-5������Fe3+�Ƿ������ȫ�IJ���Ϊ��ȡ������Һ���μӼ���KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ�����۲첻��Ѫ��ɫ����˵��Fe3+������ȫ��
�ʴ�Ϊ��8��10-5��ȡ������Һ���μӼ���KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ�����۲첻��Ѫ��ɫ����˵��Fe3+������ȫ��
��4�����������ƺͲ��ᷴӦ���ɲ����ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��2 Y��OH��2��s��+2H2C2O4��aq��=Y2��C2O4��3��s��+6H2O��l����
�ʴ�Ϊ��2 Y��OH��2��s��+2H2C2O4��aq��=Y2��C2O4��3��s��+6H2O��l����
����H2C2O4��ʪ���KClO3��ϼ��ȵ�60����Ƶù��ʹ��ϵĸ�Ч����������ClO2����Ӧ�Ļ�ѧ����ʽΪ��H2C2O4+2KClO3=2ClO2��+CO2��+K2CO3+H2O������KClO3Ϊ��������CO2��K2CO3������������������������������ʵ���֮��Ϊ1��1������ˮ�ж������Ⱥ�ˮ��Ӧ�Ļ�ѧ����ʽΪ��6ClO2+2H2O=Cl2+4HClO2+3O2��
�ʴ�Ϊ��1��1��6ClO2+2H2O=Cl2+4HClO2+3O2��
���� ���⿼�������ʷ����ᴿ�Ĺ��̷������������ʺͷ�Ӧ������жϡ�ƽ�ⳣ�����㡢������ԭ��Ӧ��ѧ����ʽ��д�͵����غ�ļ���Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | ���ǹ��ۻ����� | B�� | �������ӻ����� | C�� | �����й��ۼ� | D�� | ��Ϊͬ�������� |
| A�� | ���Ͻ� | B�� | ���Ͻ� | C�� | ͭ�Ͻ� | D�� | �� |
| ��ʼŨ�� | �� | �� | �� |
| c��NO2��/mol•L-1 | 0.10 | 0.20 | 0.20 |
| C��SO2��/mol•L-1 | 0.10 | 0.10 | 0.20 |
| A�� | �������еķ�Ӧ��ǰ2 min��ƽ������v��SO2��=0.05 mol•L-1•min-1 | |
| B�� | �ﵽƽ��ʱ��������������Ӧ��������������� | |
| C�� | �¶�����90�棬������Ӧƽ�ⳣ��Ϊ1.56����Ӧ�ġ�H��0 | |
| D�� | ������������ʼʱ�ij�0.10 mol•L-1 NO2��0.20mol•L-1 SO2���ﵽƽ��ʱc��NO����ԭƽ����ͬ |
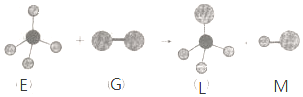
| A�� | ���³�ѹ�£�E��һ����ɫ��ζ������ | |
| B�� | �����G��Ư����ɫ���� | |
| C�� | �ڹ�������L���� G�����������������Ƶķ�Ӧ | |
| D�� | ������Ӧ������ȡ����Ӧ |
| A�� | CaCO3 | B�� | Al2O3 | C�� | Fe2O3 | D�� | MgO |
| A�� | ��״���£�1.12L ��������ԭ����Ϊ0.1NA | |
| B�� | 22.4 LHCl����ˮ����Һ��H+��ΪNA | |
| C�� | 1.6gNH2-��������������ΪNA | |
| D�� | 10g D2O������������Ϊ4.5NA |
�ף�A 2mol��B 1mol�� �ң�A 1mol��B 1mol�� ����A 2mol��B 2mol������A 1mol��B 2mol������ͬ�¶��½���ƽ��ʱ��A��B��ת���ʴ�С��ϵΪ��������
| A�� | A��ת����Ϊ�ף������ң��� | B�� | A��ת����Ϊ�ף��ң������� | ||
| C�� | B��ת����Ϊ�ף��ң������� | D�� | B��ת����Ϊ�ף������ң��� |
