题目内容
15.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、ClO- | |
| B. | Al3+能大量存在的溶液:Na+、NH4+、NO3-、I- | |
| C. | 与Al反应放出H2的溶液:Mg2+、Ca2+、NO3-、HCO3- | |
| D. | c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |
分析 A.能使pH试纸呈红色的溶液中存在大量氢离子,次氯酸根离子与氢离子、碘离子反应;
B.Al3+能大量存在的溶液可能呈酸性,酸性条件下硝酸根离子能够氧化碘离子;
C.与Al反应放出H2的溶液呈酸性或碱性,镁离子、钙离子与碳酸氢根离子、氢氧根离子反应,碳酸氢根离子与氢离子反应;
D.c(H+)/c(OH-)=1×10-12的溶液中存在的氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应.
解答 解:A.能使pH试纸呈红色的溶液呈酸性,溶液中存在大量氢离子,ClO-与H+、I-反应,在溶液中不能大量共存,故A错误;
B.Al3+能大量存在的溶液可能为酸性溶液,NO3-、I-在酸性条件下发生氧化还原反应,在酸性溶液中不能大量共存,故B错误;
C.与Al反应放出H2的溶液中存在大量氢离子或氢氧根离子,Mg2+、Ca2+与OH-、HCO3-反应生成难溶物,HCO3-与氢离子反应,在溶液中一定不能大量共存,故C错误;
D.c(H+)/c(OH-)=1×10-12的溶液呈碱性,溶液中存在大量氢氧根离子,K+、AlO2-、CO32-、Na+之间不反应,都不与氢氧根离子反应,在溶液中一定能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
3.在三个等体积的密闭容器中分别充入N2、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p),从大到小的顺序是( )
| A. | p(N2)>p(H2)>p(O2) | B. | p(O2)>p(N2)>p(H2) | C. | p(N2)>p(O2)>p(H2) | D. | p(H2)>p(N2)>p(O2) |
6.铁在高温下与水蒸气反应的固体产物是( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | Fe(OH)2 |
1.下列实验现象及相关的离子方程式均正确的是( )
| A. | 向FeCl3溶液中加入少量锌粒:2Fe3++Zn═2Fe2++Zn2+ | |
| B. | 向Ba(NO3)2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O═BaSO3↓+2H+ | |
| C. | 向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO4-+7H2O2+6H+═2Mn2++6O2↑+10H2O | |
| D. | 向FeCl3溶液中加入少量Na2S溶液:2Fe3++3S2-═Fe2S3↓ |
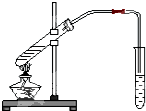 如图为实验室制乙酸乙酯的装置.
如图为实验室制乙酸乙酯的装置.