题目内容
对于反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O,以下叙述正确的是
A.Cl2是氧化剂,NaOH是还原剂
B.每生成1个的NaClO3转移10个的电子
C.Cl2既是氧化剂又是还原剂
D.被氧化的Cl原子和被还原的Cl原子之比为5∶1
练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
10.一定条件下,在容积为2L的密闭容器内发生反应:2SO2(g)+O2(g)?2SO3(g)已知起始充入4molSO2(g)和2molO2(g),经2s后测得SO3的浓度为0.6mol/L.下列说法正确的是( )
| A. | 降低体系温度能加快该反应的速率 | |
| B. | 0~2S内用O2表示该反应的平均反应速率为0.15mol/(L•s) | |
| C. | 增大SO3的浓度能减慢该反应速率 | |
| D. | 反应一段时间后可生成4molSO3 |
8.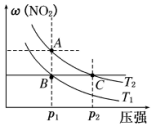 反应 N2O4(g)?2NO2(g)在温度为 T1、T2(T2>T1)时,平衡体系中 NO2的体积分数随压强变化如图所示.下列说法正 确的是( )
反应 N2O4(g)?2NO2(g)在温度为 T1、T2(T2>T1)时,平衡体系中 NO2的体积分数随压强变化如图所示.下列说法正 确的是( )
 反应 N2O4(g)?2NO2(g)在温度为 T1、T2(T2>T1)时,平衡体系中 NO2的体积分数随压强变化如图所示.下列说法正 确的是( )
反应 N2O4(g)?2NO2(g)在温度为 T1、T2(T2>T1)时,平衡体系中 NO2的体积分数随压强变化如图所示.下列说法正 确的是( )| A. | 由图可知 B 点的平衡常数大于 C 点的平衡常数 | |
| B. | A、C 两点气体的颜色:A 深,C 浅 | |
| C. | A、C 两点气体的平均相对分子质量:A<C | |
| D. | 保持容器体积不变,再充入 N2O4 气体,平衡逆向移动 |
15.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、ClO- | |
| B. | Al3+能大量存在的溶液:Na+、NH4+、NO3-、I- | |
| C. | 与Al反应放出H2的溶液:Mg2+、Ca2+、NO3-、HCO3- | |
| D. | c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |
4.欲配制下列四种无色透明的酸性溶液,其中能配制成功的是( )
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、Fe3+、OH-、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Ca2+、Mg2+、HCO3-、CO32- |
11.某粒子用Rn+表示,下列关于该粒子的叙述正确的是( )
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=Z+A |
6.下列离子方程式书写正确的是( )
| A. | 向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | CO2通入石灰乳中:CO2+Ca2++2OH-═CaCO3↓+H2O | |
| C. | 铁屑溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |

