题目内容
13.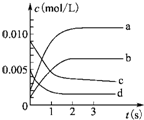 在2L密闭容器中,在800℃下反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,在800℃下反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)能使该反应的反应速率增大的是bcd.
a.及时分离出NO2气体b.适当升高温度c.增大O2的浓度d.选择高效的催化剂.
分析 (1)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=$\frac{△c}{△t}$求得NO的反应速率,再根据速率之比等于计量数之比计算O2的平均速率;
(2)根据影响化学反应速率的因素判断.
解答 解:(1)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,反应中浓度的变化量也相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=$\frac{△c}{△t}$求得NO的反应速率为$\frac{\frac{0.02-0.008}{2}}{2}$mol/(L•s)=0.003mol/(L•s),再根据速率之比等于计量数之比计算O2的平均速率为$\frac{1}{2}$×0.003mol/(L•s)=0.0015mol/(L•s),故答案为:b;0.0015mol/(L•s);
(2)a.及时分离出NO2气体,生成物浓度减小,平衡正向移动,反应物浓度也减小,所以正逆反应速率都减小;
b.适当升高温度,加快反应速率;
c.增大O2的浓度,平衡正向移动,生成物浓度增加,正逆反应速率都会加快;
d.选择高效的催化剂,可以同等程度提高正逆反应速率;
故选bcd.
点评 本题主要考查了化学反应速率的计算、影响化学反应速率的因素等知识点,中等难度,解题时注意基础知识的灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 2.4 g镁在足量的O2中燃烧,转移的电子数为0.1 NA | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2 NA | |
| C. | 1 L一氧化碳气体一定比1 L氧气的质量小 | |
| D. | 常温常压下,8 g O3中含有8 NA个电子 |
8.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)
下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.20 | a |
| ④ | 800 | 0.10 | 0.10 | b |
| A. | 实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N)=1.0×10-2mol/(L•min) | |
| B. | 实验②中,该反应的平衡常数K=2.0 | |
| C. | 实验③中,达到平衡时,X的转化率为50% | |
| D. | 实验④中,达到平衡时,b<0.05 |
18.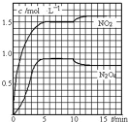 向2L 的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:①2NO(g)+O2(g)═2NO2(g)②2NO2(g)═N2O4(g)测得 NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min 后升高并维持容器的温度为T2℃.下列说法正确的是( )
向2L 的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:①2NO(g)+O2(g)═2NO2(g)②2NO2(g)═N2O4(g)测得 NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min 后升高并维持容器的温度为T2℃.下列说法正确的是( )
 向2L 的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:①2NO(g)+O2(g)═2NO2(g)②2NO2(g)═N2O4(g)测得 NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min 后升高并维持容器的温度为T2℃.下列说法正确的是( )
向2L 的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:①2NO(g)+O2(g)═2NO2(g)②2NO2(g)═N2O4(g)测得 NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min 后升高并维持容器的温度为T2℃.下列说法正确的是( )| A. | 前 5min 反应的平均速率 v(N2O4)=0.36mol•L-1•min-1 | |
| B. | T1℃时反应②的化学平衡常数K=0.6 | |
| C. | 若起始时向该容器中充入3.6molNO 2和 2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10% | |
| D. | 反应①、②均为吸热反应 |
5.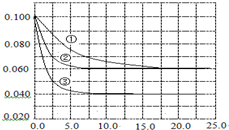 在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol•L-1,c(B)=0.200mol•L-1,c(C)=0mol•L-1.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )
在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol•L-1,c(B)=0.200mol•L-1,c(C)=0mol•L-1.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )
 在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol•L-1,c(B)=0.200mol•L-1,c(C)=0mol•L-1.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )
在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol•L-1,c(B)=0.200mol•L-1,c(C)=0mol•L-1.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )| A. | 反应A+2B?C的△H>0 | |
| B. | 若反应①、②的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 实验②平衡时B的转化率为60% | |
| D. | 减小反应③的压强,可以使平衡时c(A)=0.060 mol•L-1 |
3.一定温度下,将0.1molAgCl加入1L 0.1mol•L-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是( )
| A. | 沉淀转化反应2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol•L-1 | |
| B. | 约有2×10-5mol AgCl溶解 | |
| C. | 反应后溶液中的:c(Na+)>c (Cl-)>c (CO32-)>c (OH-)>c (H+) | |
| D. | 反应后溶液中的:c(Na+)+c (H+)+c (Ag+)=2 c (CO32-)+c (HCO3-)+c (Cl-)+c (OH-) |