题目内容
3.能正确表示下列反应的离子方程式是( )| A. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | NaHSO4溶液与Ba(OH)2溶液反应,当SO42-完全沉淀时:H++SO42-+OH-+Ba2+═BaSO4↓+H2O | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
分析 A.磁性氧化铁为四氧化三铁,属于难溶物质;
B.向Na2SiO3溶液中通入过量SO2生成NaHSO3;
C.NaHSO4溶液与Ba(OH)2溶液反应,当SO42-完全沉淀时,生成产物为BaSO4、NaOH和水;
D.Na2S2O3溶液中加入稀硫酸生成二氧化硫、S、硫酸钠和水.
解答 解:A.磁性氧化铁为四氧化三铁,属于难溶物质,四氧化三铁与稀硝酸反应生成NO、硝酸铁和水,则离子方程式为:3Fe3O4+28H++NO3-═9Fe3++NO↑+14H2O,故A错误;
B.向Na2SiO3溶液中通入过量SO2生成NaHSO3,则向Na2SiO3溶液中通入过量SO2,离子方程式为:SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3-,故B错误;
C.NaHSO4溶液与Ba(OH)2溶液反应,当SO42-完全沉淀时,生成产物为BaSO4、NaOH和水,其反应的离子方程式为:H++SO42-+OH-+Ba2+═BaSO4↓+H2O,故C正确;
D.Na2S2O3溶液中加入稀硫酸生成二氧化硫、S、硫酸钠和水,反应的离子方程式为:S2O32-+2H+═SO2↑+S↓+H2O,故D错误.
故选C.
点评 本题考查了离子方程式的正误判断,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.在一定体积的密闭容器中,进行如下化学反应:C(s)+H2O(g)?CO(g)+H2(g),其化学平衡常数K与温度t的关系如下表:
请回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)该反应的逆反应为吸热反应(选填“吸热”或“放热”).
(3)不能判断该反应是否达到化学平衡状态的依据是D.
A.容器内压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(4)某温度下,平衡浓度符合c(CO)•c(H2)=c(H2O),试判断此时的温度为830℃.
(5)为了提高H2O(g)的转化率,可以采取的措施有:①减小压强②降低温度.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)该反应的逆反应为吸热反应(选填“吸热”或“放热”).
(3)不能判断该反应是否达到化学平衡状态的依据是D.
A.容器内压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(4)某温度下,平衡浓度符合c(CO)•c(H2)=c(H2O),试判断此时的温度为830℃.
(5)为了提高H2O(g)的转化率,可以采取的措施有:①减小压强②降低温度.
14.向KOH溶液中通入8.96L(标准状况)氯气恰好完全反应生成三种含氯盐:0.6molKCl、0.1molKClO和X.则X是( )
| A. | 0.1molKClO4 | B. | 0.1molKClO3 | C. | 0.1molKClO2 | D. | 0.2molKClO |
11.镍镉电池在通讯、交通及日常生活中有着广泛的应用,其工作原理可以表示为:Cd+2NiO(OH)+2H2O?2Ni(OH)2+Cd(OH)2以下说法中正确的是( )
| A. | 以上反应是可逆反应 | |
| B. | 放电时,镉为正极 | |
| C. | 充电时电池上标有“+”号的电极连接电源正极 | |
| D. | 以镍镉电池为电源,电解Na2CO3溶液,当收集到气体的总体积为33.6L电池中转移了2mol电子 |
18.已知448℃时反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数是$\frac{1}{7}$,则H2(g)+I2(g)?2HI(g)在该温度下的平衡常数是( )
| A. | $\frac{1}{14}$ | B. | 14 | C. | $\frac{1}{49}$ | D. | 49 |
15.C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元索周期表第三周期第IVA族.
(2)N原子的原子结构示意图为 ;Cu的低价氧化物的颜色为砖红色.
;Cu的低价氧化物的颜色为砖红色.
(3)用“>”或“<”填空:
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,t1时,原电池中电子流动方向发生改变,其原因是铝在浓硝酸中发生钝化,氧化膜阻止了Al进一步发生反应,Al作正极,当硝酸浓度降为一定浓度时变为稀硝酸,Al开始做负极,电子流动方向发生改变.
(1)Si位于元索周期表第三周期第IVA族.
(2)N原子的原子结构示意图为
 ;Cu的低价氧化物的颜色为砖红色.
;Cu的低价氧化物的颜色为砖红色.(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al>Si | N<O | 金刚石>晶体硅 | CH4<SiH4 |

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,t1时,原电池中电子流动方向发生改变,其原因是铝在浓硝酸中发生钝化,氧化膜阻止了Al进一步发生反应,Al作正极,当硝酸浓度降为一定浓度时变为稀硝酸,Al开始做负极,电子流动方向发生改变.
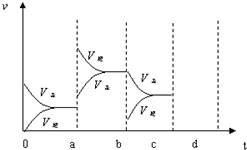 如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升温;b~c过程中改变的条件可能是减小生成物 SO3 的浓度; 若增大压强时,反应速度变化情况画在c~d处.以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).
如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升温;b~c过程中改变的条件可能是减小生成物 SO3 的浓度; 若增大压强时,反应速度变化情况画在c~d处.以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).