题目内容
关于体积相同、pH均为3的H2SO4溶液和CH3COOH溶液,下列说法正确的是( )
| A、分别与足量的Mg反应,CH3COOH溶液产生的H2多 |
| B、分别用pH=12的NaOH溶液中和,H2SO4消耗的NaOH多 |
| C、分别加入对应的钠盐固体后,二者pH仍为3 |
| D、分别加水稀释100倍后,二者的pH均变为5 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、酸的物质的量越大,和金属反应生成的氢气的量越多;
B、用pH=12的NaOH溶液中和酸,氢离子物质的量越大,消耗的碱越多;
C、醋酸是弱酸,存在电离平衡,硫酸是强酸,根据盐对电离平衡的影响知识来回答;
D、醋酸是弱酸,存在电离平衡,加水稀释会促进电离.
B、用pH=12的NaOH溶液中和酸,氢离子物质的量越大,消耗的碱越多;
C、醋酸是弱酸,存在电离平衡,硫酸是强酸,根据盐对电离平衡的影响知识来回答;
D、醋酸是弱酸,存在电离平衡,加水稀释会促进电离.
解答:
解:A、相同体积pH均为3的H2SO4溶液和CH3COOH溶液中,醋酸的物质的量大,产生的氢气量多,故A正确;
B、分别用pH=12的NaOH溶液中和,会促进醋酸的电离,所以醋酸消耗的氢氧化钠多,故B错误;
C、硫酸中加入硫酸钠固体,pH几乎不变,醋酸中加入醋酸钠,会使pH增大,故C错误;
D、硫酸加水稀释后,pH变为5,醋酸加水稀释后,pH会小于5,故D错误.
故选A.
B、分别用pH=12的NaOH溶液中和,会促进醋酸的电离,所以醋酸消耗的氢氧化钠多,故B错误;
C、硫酸中加入硫酸钠固体,pH几乎不变,醋酸中加入醋酸钠,会使pH增大,故C错误;
D、硫酸加水稀释后,pH变为5,醋酸加水稀释后,pH会小于5,故D错误.
故选A.
点评:本题考查学生弱电解质在水溶液中的电离平衡的有关知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
用下列实验装置进行相应的实验,能够达到实验目的是( )
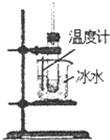 | 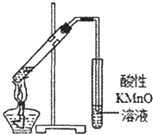 | 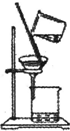 | 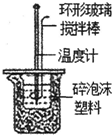 |
| A实验室制取少量的硝基苯 | B证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 | C分离乙酸乙酯、碳酸钠和水的混合物 | D在实验室测定中和反应的反应热 |
| A、A | B、B | C、C | D、D |
下列装置或操作能达到实验目的是( )
A、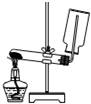 实验室制取并收集NH3 |
B、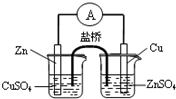 构成铜锌原电池 |
C、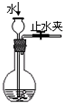 检查装置气密性 |
D、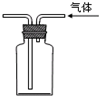 利用排空气法收集CO2 |
奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质能满足如图中阴影部分关系的是( )


| A、①NaCl;②K2SO4;③KCl;④(NH4)2SO4; |
| B、①Na2SO4;②K2SO4;③KCl;④(NH4)2SO4; |
| C、①NaCl;②K2SO4;③KCl;④NH4Cl; |
| D、①Na2SO4;②K2SO4;③KCl;④NH4Cl. |
化学在生产和日常生活中有着重要的应用.下列叙述不正确的是( )
| A、今年4月22日是第45个“世界地球日”,其活动主题为“珍惜地球资源,转变发展方式--节约集约利用国土资源共同保护自然生态空间”,我们要大量植树造林,保护土壤不流失 |
| B、将洁厕灵(主要成分:HCl)和84消毒液(主要成分:NaClO)混合使用能快速除去马桶内的污渍和异味,同时也能有效杀灭真菌和一些细菌繁殖体 |
| C、“4?11”兰州市自来水苯超标事件引发关注.我们可以将含有少量苯的饮用水煮沸3至4分钟,并将蒸发的气体通过痛风设施(排烟罩等)排除室外,从而达到消除水中的苯 |
| D、PX即“对二甲苯”.前段时间,清华学子捍卫毒性之争引发的PX“词条保卫战”,最终让百度词条锁定PX为“低毒化合物”.这充分反映了去伪存真的科学精神 |
设NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
下列叙述正确的是( )
| A、烧碱、小苏打、醋酸、次氯酸均为电解质 |
| B、碘酒、牛奶、豆浆、蔗糖水均为胶体 |
| C、是否具有丁达尔效应是区分溶液、胶体和浊液的本质原因 |
| D、物质可根据在水中或熔化状态下的导电性分为电解质与非电解质 |
下列物质:①水泥 ②玻璃 ③陶瓷 ④水晶,其中属于硅酸盐工业产品的是( )
| A、只有①② | B、只有②④ |
| C、只有①②③ | D、全部 |