题目内容
下列各反应,能用同一离子方程式表示的是( )
| A、氢氧化铜与盐酸、氢氧化铜与醋酸 |
| B、氯化钡溶液与硫酸铜溶液、氢氧化钡溶液与硫酸铜溶液 |
| C、氢氧化钡与稀硫酸、氢氧化钡与稀盐酸 |
| D、石灰石与稀硝酸、石灰石与稀盐酸 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.醋酸是弱电解质写化学式,HCl是强电解质,写离子;
B.氢氧化钡和硫酸铜溶液反应还生成氢氧化铜沉淀;
C.氢氧化钡和硫酸铜溶液反应还生成硫酸钡沉淀;
D.硝酸和HCl都是强电解质,写离子.
B.氢氧化钡和硫酸铜溶液反应还生成氢氧化铜沉淀;
C.氢氧化钡和硫酸铜溶液反应还生成硫酸钡沉淀;
D.硝酸和HCl都是强电解质,写离子.
解答:
解:A.氢氧化铜与盐酸、氢氧化铜与醋酸反应的离子方程式分别为:Cu(OH)2+2H+=Cu2++2H2O、Cu(OH)2+2CH3COOH=Cu2++2CH3COO-+2H2O,所以离子方程式不同,故A错误;
B.氯化钡溶液与硫酸铜溶液、氢氧化钡溶液与硫酸铜溶液反应离子方程式分别为:Ba2++SO42-=BaSO4↓、Ba2++2OH-+SO42-+Cu2+=BaSO4↓+Cu(OH)2↓,所以离子方程式不同,故B错误;
C.氢氧化钡与稀硫酸、氢氧化钡与稀盐酸反应离子方程式分别为:Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O、OH-+H+=H2O,所以离子方程式不同,故C错误;
D.硝酸和HCl都是强电解质,写离子,其离子方程式都是CaCO3+2H+=Ca2++CO2↑+H2O,所以离子方程式相同,故D正确;
故选D.
B.氯化钡溶液与硫酸铜溶液、氢氧化钡溶液与硫酸铜溶液反应离子方程式分别为:Ba2++SO42-=BaSO4↓、Ba2++2OH-+SO42-+Cu2+=BaSO4↓+Cu(OH)2↓,所以离子方程式不同,故B错误;
C.氢氧化钡与稀硫酸、氢氧化钡与稀盐酸反应离子方程式分别为:Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O、OH-+H+=H2O,所以离子方程式不同,故C错误;
D.硝酸和HCl都是强电解质,写离子,其离子方程式都是CaCO3+2H+=Ca2++CO2↑+H2O,所以离子方程式相同,故D正确;
故选D.
点评:本题考查离子方程式的书写,明确物质的溶解性、物质的性质及离子方程式书写规则即可解答,注意硫酸铜与氢氧化钡溶液的反应,很容易漏掉生成硫酸钡或氢氧化铜沉淀,为易错点.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
设NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
以下实验操作正确的是( )
A、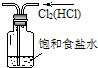 除去Cl2中的HCl气体 |
B、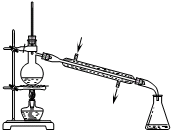 淡化海水 |
C、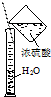 稀释浓硫酸 |
D、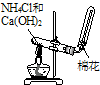 验室制取氨气 |
下列基本实验操作正确的是( )
| A、.稀释浓硫酸时将水沿器壁缓慢注入浓硫酸中,同时不断搅拌 |
| B、.过滤时,滤纸的边缘要高于漏斗的边缘 |
| C、.胶头滴管的尖嘴部分直接伸入试管里滴加液体 |
| D、实验室取用液体药品做性质实验时,如果没有说明用量,一般取1~2mL |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42-=0.2mol/L,当加等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的浓度是( )
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.45 mol/L |
| D、0.225 mol/L |