题目内容
1.如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( )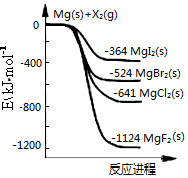
| A. | 卤素单质(X2)与水反应均可生成两种酸 | |
| B. | 用电子式表示MgF2的形成过程为: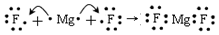 | |
| C. | 热稳定性:MgI2>MgBr2>MgCl2>MgF2 | |
| D. | 由图可知此温度下MgI2(s)与Cl2(g)反应的热化学方程式为:MgI2(s)+Cl2(g)═MgCl2(s)+I2(g),△H=-277kJ•mol-1 |
分析 A.氟气与水反应方程式:2F2+2H2O=4HF+O2;
B.用电子式表示MgF2的形成过程为: ;
;
C.物质能量越高越活泼,越不稳定;
D.反应的焓变=生成物总焓-反应物总焓.
解答 解:A.氟气与水反应方程式:2F2+2H2O=4HF+O2,不符合X2+H2O═HXO+HX,故A错误;
B.用电子式表示MgF2的形成过程为: ,故B错误;
,故B错误;
C.物质的能量越低越稳定,易图象数据分析,化合物的热稳定性顺序为:MgI2<MgBr2<MgCl2<MgF2,故C错误;
D.反应的焓变=生成物总焓-反应物总焓;MgI2(s)的能量低于MgCl2(s),依据图象数据分析计算可知反应的焓变等于-277KJ/mol,故D正确;
故选D.
点评 本题考查了反应焓变的判断计算,物质能量越高越活泼,能量守恒是解题关键,本题题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.两种气态烃的混合气1L,完全燃烧后,生成2LCO2和2L水蒸气(相同状况),则该混合烃的组合及其体积比是( )
| A. | 甲烷和丙烯,体积比2:1 | B. | 丙烷和乙烯,体积比2:1 | ||
| C. | C2H6和C2H2,体积比为1:1 | D. | C2H6和C2H2,体积比2:1 |
12.短周期元素X、Y、Z、W、M的原子序数依次增大,且原子最外层电子数之和为18,X与Y是组成化合物种类最多的元素,W是地壳中含量最高的元素.下列说法正确的是( )
| A. | 原子半径大小顺序:r(Y)>r(Z )>r(W)>r(M) | |
| B. | Z的气态氢化物比W的气态氢化物更稳定 | |
| C. | 分子式为Y5X12的物质只有3种 | |
| D. | 由三种元素X、Z、W形成的化合物中只有共价键而无离子键 |
16.设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 在含A13+总数为NA的A1C13溶液中,C1-总数为3NA | |
| B. | 标准状况下,5.6L CO2中含有的共用电子对数为0.5NA | |
| C. | Na2O2与足量的CO2反应生成0.1mol O2,转移的电子数为0.2NA | |
| D. | 常温下,56g铁片投入足量浓H2SO4中,充分反应,生成NA个SO2分子 |
13.下列有关化学与生产、生活的说法中,正确的是( )
| A. | 碳纤维、合成纤维和光导纤维都是无机非金属材料 | |
| B. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| C. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力增强 | |
| D. | 铝合金的大量使用归功于人们能使用焦炭从氧化铝中获得铝 |
10.已知X+Y→M+N反应中的能量变化过程如图,则下列推断一定正确的是( )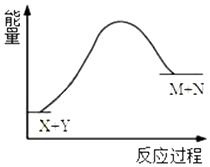

| A. | X的能量低于M的能量 | |
| B. | Y的能量低于N的能量 | |
| C. | X和Y总能量低于M和N总能量 | |
| D. | 该反应是吸热反应,反应条件是加热 |
12.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 物 质 | 试 剂 | 分 离 方 法 | |
| A. | Cl2(HCl) | 饱和碳酸氢钠溶液 | 洗气 |
| B. | 硬脂酸钠(甘油) | 饱和食盐水 | 盐析后过滤 |
| C. | KNO3(KCl) | 水 | 蒸发结晶 |
| D. | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |