题目内容
10.已知X+Y→M+N反应中的能量变化过程如图,则下列推断一定正确的是( )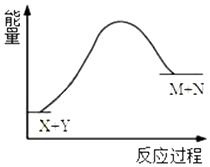
| A. | X的能量低于M的能量 | |
| B. | Y的能量低于N的能量 | |
| C. | X和Y总能量低于M和N总能量 | |
| D. | 该反应是吸热反应,反应条件是加热 |
分析 A.由图可知,生成物的总能量大于反应物的总能量,而不是某一种反应物或生成物的能量关系;
B.由图可知,生成物的总能量大于反应物的总能量,而不是某一种反应物或生成物的能量关系;
C.由图可知,X和Y总能量低于M和N总能量;
D.反应物的总能量低于生成物的总能量是吸热反应,反应放热还是吸热与条件没有关系.
解答 解:A.由图可知,M和N的总能量大于X和Y的总能量,不能说明X的能量一定低于M的能量,故A错误;
B.由图可知,M和N的总能量大于X和Y的总能量,Y的能量一定低于N的能量,故B错误;
C.由图可知,X和Y总能量低于M和N总能量,故C正确;
D.反应物的总能量低于生成物的总能量是吸热反应,但是反应放热还是吸热与条件没有关系,故D错误,
故选C.
点评 本题考查吸热反应与放热反应,可以根据能量守恒从反应物与生成物的总能量、化学键的断裂与形成两个角度进行理解,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列反应中酸既表现氧化性又表现酸性的是( )
| A. | MnO2和浓HCl | B. | Cu和稀HNO3 | C. | C和浓H2SO4 | D. | Cu(OH)2和稀HNO3 |
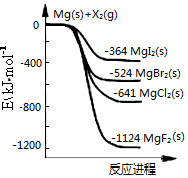
1.如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( )

| A. | 卤素单质(X2)与水反应均可生成两种酸 | |
| B. | 用电子式表示MgF2的形成过程为: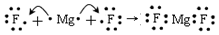 | |
| C. | 热稳定性:MgI2>MgBr2>MgCl2>MgF2 | |
| D. | 由图可知此温度下MgI2(s)与Cl2(g)反应的热化学方程式为:MgI2(s)+Cl2(g)═MgCl2(s)+I2(g),△H=-277kJ•mol-1 |
18.H2S燃料电池应用前景非常广阔,该电池示意图如下.下列说法正确的是( )
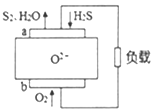

| A. | 电极a是正极 | |
| B. | O2-由电极a移向电极b | |
| C. | 电极 a 的反应式为:2H2S+2O2--4e-═S2+2H2O | |
| D. | 当通入1.12LO2,转移电子数0.2NA |
5.保存液态有机物的一种方法是在其上方加盖一层水以避免挥发损失.下列有机物适合用“水封法”保存的是( )
| A. | 乙醇 | B. | 硝基苯 | C. | 甘油 | D. | 己烷 |
15.用 NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1AlCl3 溶液中,含 Al3+数目小于 NA | |
| B. | 标准状况下,6.0gNO 和 2.24LO2混合,所得气体的分子数目为 0.2NA | |
| C. | 25℃,1LpH=1 的稀硫酸中含有的 H+数为 0.2NA | |
| D. | 由 1molCH3COONa 和少量 CH3COOH 形成的中性溶液中,CH3COO-数目为NA 个 |
3.下列条件变化,一定使任何反应的正、逆反应速率都增大的是( )
| A. | 缩小反应容器的体积 | B. | 增加反应物的物质的量 | ||
| C. | 升高温度 | D. | 增加催化剂的用量 |
1.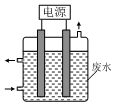 用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
 用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )| A. | 除去CN-的反应:2CN-+5ClO-+2H+═N2↑+2CO2↑+5Cl-+H2O | |
| B. | 阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O | |
| C. | 阴极的电极反应式为:2H2O+2e-═H2↑+2OH- | |
| D. | 用石墨作阳极,铁作阴极 |
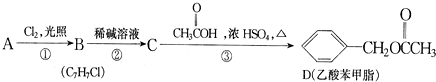
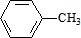 、
、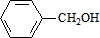 .
.
 、
、 .
.