题目内容
11.两种气态烃的混合气1L,完全燃烧后,生成2LCO2和2L水蒸气(相同状况),则该混合烃的组合及其体积比是( )| A. | 甲烷和丙烯,体积比2:1 | B. | 丙烷和乙烯,体积比2:1 | ||
| C. | C2H6和C2H2,体积比为1:1 | D. | C2H6和C2H2,体积比2:1 |
分析 两种气态烃的混合气1L,完全燃烧后,生成2LCO2和2L水蒸气(相同状况),则平均分子式为C2H4,据此判断各选项组成情况,根据组成中C原子或H原子数目计算体积之比,据此进行解答.
解答 解:两种气态烃的混合气1L,完全燃烧后,生成2LCO2和2L水蒸气(相同状况),则平均分子式为C2H4,
A.若为CH4和C3H6混合,设CH4和C3H6的物质的量分别为x mol、ymol,由C原子平均可知:$\frac{x+3y}{x+y}$=2,解得x:y=1:1,即二者体积之比为1:1,二者1:1混合,平均H原子数目=$\frac{4+6}{2}$=5,平均H原子数目不是4,不符合,故A错误;
B.C3H8和C2H4混合,平均C原子数目介于2~3之间,平均H原子数目介于4~8之间,不符合,故B错误;
C.C2H6和C2H2混合,由平均C原子数目,二者为任意比,设C2H6和C2H2的物质的量分别为x mol、ymol,由H原子平均可知:$\frac{6x+2y}{x+y}$=4,解得x:y=1:1,即二者体积之比为1:1,符合题意,故C正确;
D.由C中分析可知,C2H6和C2H2混合,体积之比应该为1:1,故D错误;
故选C.
点评 本题考查混合物的计算,题目难度中等,注意利用平均分子式进行解答,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
1.下列所得溶液的物质的量浓度等于0.1mol•L-1的是( )
| A. | 将0.1 mol HCl充分溶解在1 L水中 | |
| B. | 将60 g质量分数为10%的醋酸与940 g水混合 | |
| C. | 将3.1 g氧化钠溶于水并配成1 L溶液 | |
| D. | 将14.2 g Na2SO4•10H2O溶于水中配成1 L溶液 |
2.为了提纯表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | 酸性KMnO4溶液 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(甲苯) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
16.有关HF和HCl判断正确的是( )
| A. | 键长:HF>HCl | B. | 键能:HF>HCl | ||
| C. | 稳定性:HCl>HF | D. | 共用电子对偏移程度:HCl>HF |
20.下列反应中酸既表现氧化性又表现酸性的是( )
| A. | MnO2和浓HCl | B. | Cu和稀HNO3 | C. | C和浓H2SO4 | D. | Cu(OH)2和稀HNO3 |
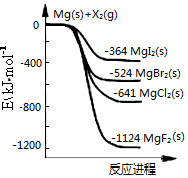
1.如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( )

| A. | 卤素单质(X2)与水反应均可生成两种酸 | |
| B. | 用电子式表示MgF2的形成过程为: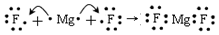 | |
| C. | 热稳定性:MgI2>MgBr2>MgCl2>MgF2 | |
| D. | 由图可知此温度下MgI2(s)与Cl2(g)反应的热化学方程式为:MgI2(s)+Cl2(g)═MgCl2(s)+I2(g),△H=-277kJ•mol-1 |
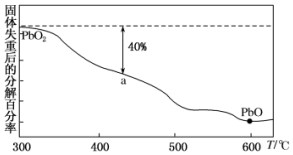 已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等.
已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等.