题目内容
下列对图象描述正确的是( )
A、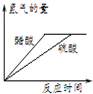 图表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系 |
B、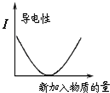 图表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系 |
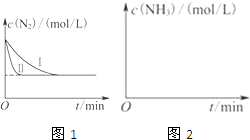
C、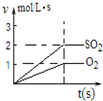 图表示2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率大小关系 |
D、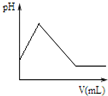 图表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系 |
考点:弱电解质在水溶液中的电离平衡,化学反应速率与化学平衡图象的综合应用,电解质溶液的导电性
专题:
分析:A、体积和pH值均相同的稀硫酸和醋酸与足量的镁反应,醋酸生成的氢气多;
B、向NaOH溶液中滴加稀盐酸生成氯化钠,溶液导电性变化不大;
C、2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率之比始终为2:1;
D、向氨水中滴加稀硫酸时,溶液的pH变小.
B、向NaOH溶液中滴加稀盐酸生成氯化钠,溶液导电性变化不大;
C、2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率之比始终为2:1;
D、向氨水中滴加稀硫酸时,溶液的pH变小.
解答:
解:A、体积和pH值均相同的稀硫酸和醋酸与足量的镁反应,醋酸生成氢气的速率快且多,故A错误;
B、向NaOH溶液中滴加稀盐酸生成氯化钠,溶液导电性变化不大,故B错误;
C、2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率之比始终为2:1,故C正确;
D、向氨水中滴加稀硫酸时,溶液的pH变小,故D错误;
故选C.
B、向NaOH溶液中滴加稀盐酸生成氯化钠,溶液导电性变化不大,故B错误;
C、2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率之比始终为2:1,故C正确;
D、向氨水中滴加稀硫酸时,溶液的pH变小,故D错误;
故选C.
点评:本题考查了图象问题,注意分析图象的坐标和图象的起点、拐点和终点,题目难度不大.

练习册系列答案
相关题目
“文房四宝”是中华文明的杰出代表,其制作原料或成分分别为:笔(主要是动物毛发)、墨(炭墨烟和动物胶)、纸(植物纤维)、砚(主要成分是硅酸盐).下列说法中不正确的是( )
| A、纸的主要成分属于糖类 |
| B、笔和墨的原料中都存在蛋白质 |
| C、“文房四宝”中只有砚的成分中存在无机物 |
| D、笔、墨、纸、砚中都存在可能发生水解反应的物质 |
13C-NMR(核磁共振)可用于含碳化合物的结构分析,有关13C的说法正确的是( )
| A、质子数为6 |
| B、电子数为13 |
| C、中子数为6 |
| D、质量数为6 |
一定量的氧气中含有1mol电子,这些氧气的物质的量为( )
| A、1mol |
| B、0.5mol |
| C、0.125mol |
| D、0.0625mol |
下列烷烃中,常温下呈气态的是( )
| A、十七烷 | B、正已烷 |
| C、异丁烷 | D、正戊烷 |
下列图示关系中不正确的是( )
A、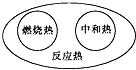 |
B、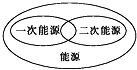 |
C、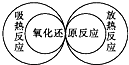 |
D、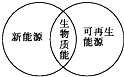 |
 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
