题目内容
 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:①CO(g)+2H2(g)?CH3OH(g)△H1=-Q1 kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-Q2 kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-Q3 kJ?mol-1
回答下列问题:
(1)新工艺的总反应3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g)的热化学方程式为
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH (g)△H
下表所列数据是该反应在不同温度下的化学平衡常数(Κ).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
A.体系的压强不变
B.密度不变
C.混合气体的相对分子质量不变
D.c(CO)=c(CH3OH)
②某温度下,将 2mol CO和 6mol H2 充入2L的密闭容器中,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K=
(3)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨.合成氨反应原理为:N2(g)+3H2(g)
| 一定条件 |
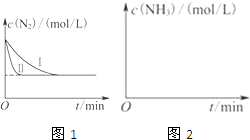
①与实验Ⅰ比较,实验Ⅱ改变的条件为
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在图2中画出实验I和实验Ⅲ中NH3浓度随时间变化的示意图.
考点:用化学平衡常数进行计算,用盖斯定律进行有关反应热的计算,化学平衡状态的判断,物质的量或浓度随时间的变化曲线
专题:
分析:(1)根据盖斯定律可写出热化学方程式;
(2)①根据温度对平衡常数的影响判断反应的热效应,根据平衡状态的特征判断平衡状态;
②根据平衡常数的定义计算平衡常数;
(3)①根据图象可知,实验Ⅱ与实验Ⅰ相比,反应达到平衡的时间变短,平衡不移动,据此判断;
②根据温度对平衡移动的影响可画出图象;
(2)①根据温度对平衡常数的影响判断反应的热效应,根据平衡状态的特征判断平衡状态;
②根据平衡常数的定义计算平衡常数;
(3)①根据图象可知,实验Ⅱ与实验Ⅰ相比,反应达到平衡的时间变短,平衡不移动,据此判断;
②根据温度对平衡移动的影响可画出图象;
解答:
解:(1)根据盖斯定律,①×2+②+③,整理可得:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-(2Q1+Q2+Q3) kJ/mol,
故答案为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-(2Q1+Q2+Q3)kJ/mol;
(2)①升高温度,化学平衡常数减小,说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应,所以△H<0;
A.由于该反应是反应前后气体体积不等的反应,若未达到平衡,则体系的压强就会发生改变,所以体系的压强不变,则反应达到平衡状态,正确;
B.密度不变由于反应混合物都是气体,所以在任何时刻物质的密度都不发生变化,因此不能作为判断平衡的标志,错误;
C.由于该反应是反应前后气体体积不等的反应,若未达到平衡,则体系的气体的物质的量就会发生变化,气体的相对分子质量就会改变,若气体的相对分子质量不变,则反应达到平衡状态,正确;
D.c(CO)=c(CH3OH)时反映可能处于平衡状态,也可能未达到平衡,因此不能作为判断平衡的标志,错误;
故答案为:<; A、C;
②某温度下,在反应开始是c(CO)=1.0mol/L,c(H2)=3.0mol/L,将 2mol CO和 6mol H2,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,则平衡时c(H2)=1.4mol/L,c(CH3OH)=0.8mol/L,则此温度下的平衡常数K=
=
=2.04,
故答案为:2.04;
(3)①根据图象可知:与实验Ⅰ比较,实验Ⅱ反应速率大大加快,达到平衡所需要的时间缩短,但是N2平衡浓度没有改变,因此平衡未发生移动,则改变的条件为加入催化剂,
故答案为:加入催化剂;
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,由于升高温度化学反应速率加快,达到平衡所需要的时间缩短,但是由于该反应是放热反应,升高温度,平衡向吸热的逆反应方向移动,因此达到平衡时NH3的含量降低,用图象表示实验I和实验Ⅲ中NH3浓度随时间变化的示意图是 ,
,
故答案为: .
.
故答案为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-(2Q1+Q2+Q3)kJ/mol;
(2)①升高温度,化学平衡常数减小,说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应,所以△H<0;
A.由于该反应是反应前后气体体积不等的反应,若未达到平衡,则体系的压强就会发生改变,所以体系的压强不变,则反应达到平衡状态,正确;
B.密度不变由于反应混合物都是气体,所以在任何时刻物质的密度都不发生变化,因此不能作为判断平衡的标志,错误;
C.由于该反应是反应前后气体体积不等的反应,若未达到平衡,则体系的气体的物质的量就会发生变化,气体的相对分子质量就会改变,若气体的相对分子质量不变,则反应达到平衡状态,正确;
D.c(CO)=c(CH3OH)时反映可能处于平衡状态,也可能未达到平衡,因此不能作为判断平衡的标志,错误;
故答案为:<; A、C;
②某温度下,在反应开始是c(CO)=1.0mol/L,c(H2)=3.0mol/L,将 2mol CO和 6mol H2,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,则平衡时c(H2)=1.4mol/L,c(CH3OH)=0.8mol/L,则此温度下的平衡常数K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.8 |
| 0.2×1.42 |
故答案为:2.04;
(3)①根据图象可知:与实验Ⅰ比较,实验Ⅱ反应速率大大加快,达到平衡所需要的时间缩短,但是N2平衡浓度没有改变,因此平衡未发生移动,则改变的条件为加入催化剂,
故答案为:加入催化剂;
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,由于升高温度化学反应速率加快,达到平衡所需要的时间缩短,但是由于该反应是放热反应,升高温度,平衡向吸热的逆反应方向移动,因此达到平衡时NH3的含量降低,用图象表示实验I和实验Ⅲ中NH3浓度随时间变化的示意图是
 ,
,故答案为:
 .
.
点评:本题主要考查热化学方程式的书写、反应热效应的判断、平衡状态的判断、催化剂、温度对平衡移动的影响的图象法表示、化学平衡常数的计算的知识,中等难度,答题时注意对平衡常数的理解和平衡移动原理的灵活运用.

练习册系列答案
相关题目
煤或石油的加工方法中,可用于大量获取乙烯和丙烯的是( )
| A、煤的干馏 |
| B、重油裂解 |
| C、石油减压分馏 |
| D、石油常压分馏 |
下列说法中,不正确的是( )
| A、“血液透析”利用了胶体的性质 |
| B、根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 |
| C、明矾[KAl(SO4)2?12H2O]净水是利用明矾与水反应生成Al(OH)3胶体,吸附了水中的悬浮物并沉降 |
| D、溶液一定是无色透明的混合物 |
下列叙述正确的是( )
| A、氢氧化钠的摩尔质量是40g |
| B、1mol NaOH的质量是40g/mol |
| C、1g H2和1g N2所含分子数相等 |
| D、等质量的N2、CH4、CO、H2O中CH4所含分子数最多 |
下列对图象描述正确的是( )
A、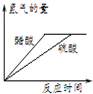 图表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系 |
B、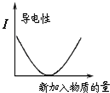 图表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系 |
C、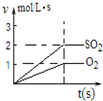 图表示2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率大小关系 |
D、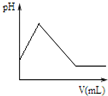 图表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系 |
已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡:下列有关说法正确的是( )
①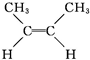 (g)?
(g)?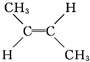 (g)△H=-4.2kJ?mol-1
(g)△H=-4.2kJ?mol-1
顺-2-丁烯 反-2-丁烯
②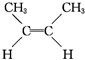 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
(g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
①
 (g)?
(g)? (g)△H=-4.2kJ?mol-1
(g)△H=-4.2kJ?mol-1顺-2-丁烯 反-2-丁烯
②
 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
(g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.| A、顺-2-丁烯比反-2-丁烯稳定 |
| B、1 mol反-2-丁烯完全燃烧生成CO2和液态水所放出的热量比顺-2-丁烯的大 |
| C、28 g顺-2-丁烯完全氢化生成丁烷气体时所放出的热量为118.9 kJ |
D、反-2-丁烯氢化的热化学方程式为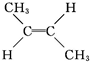 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-112.7 kJ?mol-1 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-112.7 kJ?mol-1 |
下列说法中正确的是( )
| A、在氧化还原反应中,一定是一种元素被氧化,另一种元素被还原 |
| B、在氧化还原反应中,不一定所有元素的化合价都发生改变 |
| C、有单质参加反应或有单质生成的反应一定是氧化还原反应 |
| D、某元素由化合态转化为游离态,这种元素一定被还原了 |
金属键的形成是通过( )
| A、金属原子与自由电子之间的相互作用 |
| B、金属离子与自由电子之间强烈的相互作用 |
| C、自由电子之间的相互作用 |
| D、金属离子之间的相互作用 |