题目内容
下列烷烃中,常温下呈气态的是( )
| A、十七烷 | B、正已烷 |
| C、异丁烷 | D、正戊烷 |
考点:饱和烃与不饱和烃
专题:
分析:常温下,碳原子小于等于4的烷烃是气态,大于4个碳原子的烷烃不是气态.
解答:
解:常温下,碳原子小于等于4的烷烃是气态,大于4个碳原子的烷烃不是气态,所以正戊烷(C5H12)、正己烷(C6H14)、十七烷(C17H36)都不是气体,只有异丁烷(C4H10),即2-甲基丙烷是气体,故选:C.
点评:本题考查了烷烃在常温下的状态,常温下,碳原子小于等于4的烷烃是气态,大于4个碳原子的烷烃不是气态,较简单.

练习册系列答案
相关题目
下列有机物能发生水解反应生成醇的是( )
| A、CH3CH2Br |
| B、CH2Cl2 |
| C、CHCl3 |
| D、C6H5Br |
已知:在同一个反应中,氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性.在一定条件下KClO3与I2按下式反应:2KClO3+I2═2KIO3+Cl2,下列判断正确的是( )
| A、该反应属于置换反应 |
| B、氧化性:I2>KClO3 |
| C、还原性:KClO3>I2 |
| D、还原剂为I2,氧化剂为KClO3 |
下列微粒可以在水中大量共存的是( )
| A、C6H12O6(葡萄糖)、Ag(NH3)2+、NO3-、OH- |
| B、AgI、Cl-、SO42-、NH4+ |
| C、Fe3+、K+、ClO-、NO3- |
| D、H2O2、Cl-、SO42-、Fe3+ |
下列说法正确的是( )
| A、6.02×1023个碳原子的质量为1g |
| B、钠原子的摩尔质量为23g |
| C、HCl的摩尔质量等于6.02×1023个HCl分子的质量 |
| D、Na2O2的摩尔质量为78g/mol |
下列对图象描述正确的是( )
A、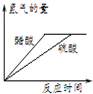 图表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系 |
B、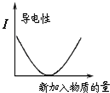 图表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系 |
C、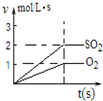 图表示2SO2(g)+O2(g)?2SO3(g)反应过程中,SO2和O2反应速率大小关系 |
D、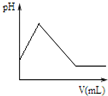 图表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系 |
在世界海运史上曾发生过这样一个悲剧:一艘名叫“阿那吉纳号”的货轮满载着精铜砂,在向日本海岸行驶时突然发生大面积漏水,最终沉没.坚硬的钢制船体为什么会突然漏水呢?事后的事故调查结果表明导致沉船的原因与船上的精铜砂密切相关.下列对此调查结论的理解正确的是( )
| A、精铜砂装载过多导致沉船 |
| B、运输途中铜与空气中的氧气发生氧化反应导致质量增大超过船的承载能力 |
| C、在潮湿的环境中,船体与铜构成了原电池,加速了作为负极的船体的腐蚀 |
| D、在潮湿的环境中,船体与铜构成了电解池,钢制船体作阳极而被氧化腐蚀 |
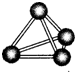 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如右图所示,下列说正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如右图所示,下列说正确的是( )| A、N4分子属于一种新型的化合物 |
| B、N4分子中只含有非极性键 |
| C、1 mol N4分子所含共价键数为4NA |
| D、N4沸点比P4(白磷)高 |
为了能够让制得的Fe(OH)2不被空气氧化 某同学采用如图所示装置进行实验,下列分析错误的是 ( )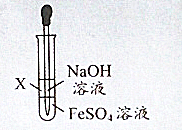

| A、该实验中NaOH溶液往往事先煮沸下,目的是为了赶走其中溶有的O2 |
| B、试剂X可以是食用油、苯或乙醇 |
| C、该实验能较长时间观察到白色沉淀的现象 |
| D、该反应的离子方程式为:Fe2++2OH-=Fe(OH)2↓ |