题目内容
19.将BaO2放入密闭真容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )| A. | 平衡常数减小 | B. | BaO量不变 | C. | 氧气压强不变 | D. | 氧气的浓度变大 |
分析 保持温度不变,缩小容器体积,增大压强,平衡向气体体积减小的方向进行,反应2BaO2(s)?2BaO(s)+O2(g)是气体体积增大的反应,增大压强该可逆反应向逆反应方向移动,化学平衡常数只与温度有关,依据平衡常数表达式分析氧气的浓度变化,据此分析选项解答.
解答 解:A.化学平衡常数只与温度有关,保持温度不变,缩小容器容积,温度不变平衡常数不变,故A错误;
B.缩小容器体积,增大压强,平衡向逆反应方向移动,则BaO的量减小,故B错误;
C.平衡向逆反应方向移动,但温度不变,平衡常数不变,氧气浓度不变,其压强不变,故C正确;
D.平衡向逆反应方向移动,但温度不变,K=[O2],平衡常数不变,氧气浓度不变,故D错误;
故选C.
点评 本题考查了可逆反应平衡移动,根据压强与平衡移动方向之间的关系分析解答即可,注意平衡常数只与温度有关,与物质浓度无关,题目难度中等.

练习册系列答案
相关题目
10.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8NA | |
| B. | 一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA | |
| C. | 1.8g重水(D2O)中含有的质子数和电子数均为NA | |
| D. | 标准状况下,22.4L NO 和22.4L O2混合后所得气体中分子总数为1.5NA |
7.在水溶液中能大量共存的离子组是( )
| A. | Mg2+、Cl-、OH- | B. | Na+、CO32-、OH- | C. | Fe2+、H+、CO32- | D. | Fe3+、K+、OH- |
4.二氧化硅是酸酐的原因是( )
| A. | 它溶于水得到相应的酸 | B. | 它对应的水化物是可溶性强酸 | ||
| C. | 它与强碱反应只生成盐和水 | D. | 它是非金属氧化物 |
5.下列化学用语正确的是( )
| A. | Cl-的结构示意图: | |
| B. | 乙酸的结构示意图:C2H4O2 | |
| C. | 硫酸的电离方程式:H2SO4═H2++SO42- | |
| D. | 氯化钠的电子式: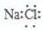 |
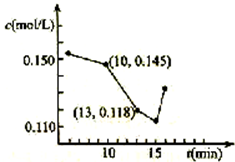 对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下:
对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下: