题目内容
3.标况下,0.1mol某烃在足量氧气中完全燃烧生成4.48L CO2和3.6g水.试求:(1)该烃的分子式;
(2)写出该烃可能的结构式.
分析 根据二氧化碳的体积以及水的质量计算C、H的物质的量,可计算1mol有机物含有C、H的物质的量,进而确定分子式,结合分子式确定可能的结构式.
解答 解:(1)n(CO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,则n(C)=0.2mol,n(H)=0.4mol,所以分子式为C2H4,
答:该烃的分子式为C2H4;
(2)该烃为乙烯,结构式为 ,答:该烃可能的结构式为
,答:该烃可能的结构式为 .
.
点评 本题考查了有机物分子式、结构简式的确定,侧重学生的分析、计算能力的考查,题目难度中等,熟练掌握常见有机物结构与性质为解答关键,注意明确质量守恒在确定有机物分子式中的应用.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
11.关于如图所示装置的叙述,正确的是( )


| A. | 此装置为原电池,铜片上有气泡产生 | |
| B. | 铜片质量逐渐减少 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 氢离子在铜片表面被氧化 |
18.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| B. | 在2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 用硝酸铜溶液代替硫酸铜溶液进行实验,不能观察到同样的现象 | |
| D. | 沉淀溶解后,将生成深蓝色的配合离子 |
8. 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )| A. | 过氧化氢分子中含有H-H键、O-O键 | |
| B. | 过氧化氢分子中存在离子键和共价键 | |
| C. | 过氧化氢分子中只有共价键,其电子式为 | |
| D. | H2O2与H2O互为同位素 |
12.两种气态烃的混合物共1mol,在空气中完全燃烧生成2mol CO2气体和2.5mol水蒸气(气体体积均在相同状况下测定),关于该混合气体的说法正确的是( )
| A. | 一定含有乙烯 | |
| B. | 可能为等物质的量甲烷和丙烯的混合物 | |
| C. | 可能为乙烷和丙烷的混合物 | |
| D. | 一定为乙烯和甲烷的混合物 |


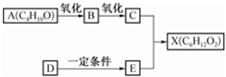 如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图:
如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图: .
.