题目内容
4.铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )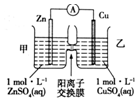
| A. | 锌电极上发生的反应: | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 电流由锌电极经电流表流向铜电极 | |
| D. | 电池工作一段时间后,乙池溶液的总质量增加 |
分析 由图象可知,该原电池反应式为:Zn+Cu2+=Zn2++Cu,Zn发生氧化反应,为负极,Cu电极上发生还原反应,为正极,阳离子交换膜只允许阳离子和水分子通过,两池溶液中硫酸根浓度不变,随反应进行,甲池中的Zn2+通过阳离子交换膜进入乙池,以保持溶液呈电中性,据此解答.
解答 解:A.由图象可知,该原电池反应式为:Zn+Cu2+=Zn2++Cu,Zn为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,故A错误;
B.阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO42-)不变,故B错误;
C.电流从正极铜极经过导线移向负极锌极,故C错误;
D.随反应进行,甲池中的Zn2+通过阳离子交换膜进入乙池,以保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增加,故D正确;
故选D.
点评 本题考查原电池工作原理,注意阳离子交换膜不允许阳离子通过,D选项利用电荷守恒分析,难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
15.最近医学界通过用放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS).下列有关14C的叙述正确的是( )
| A. | 14C与C60中普通碳原子的化学性质不同 | |
| B. | 14C与14N含的中子数相同 | |
| C. | 14C是C60的同素异形体 | |
| D. | 14C与12C互为同位素 |
12.用铝片和稀硫酸反应制取氢气时,下列做法能加快化学反应速率的是(
| A. | 用98%的浓硫酸替代稀硫酸 | B. | 降低温度 | ||
| C. | 用铝粉代替铝片 | D. | 加入Na2SO4溶液 |
19.一定条件下,在密闭容器中充入1mol N2和3mol H2进行如下反应:N2(g)+3H2(g)?2NH3(g),当N2、H2、NH3的浓度不再改变时,下列说法正确的是( )
| A. | N2、H2完全反应生成2mol NH3 | B. | N2、H2、NH3的浓度一定相等 | ||
| C. | 反应已达到化学平衡状态 | D. | 正、逆反应速率相等且等于零 |
9.下列变化中,不属于化学变化的是( )
| A. | 石墨变成金刚石 | B. | 胆矾(CuSO4•5H2O)失去结晶水 | ||
| C. | 氯气变成液氯 | D. | 白磷转化为红磷 |
14.化学与人类生产、生活、社会可持续发展密切相关.下列说法中正确的是( )
| A. | Al2(SO4)3可以除去酸性废水中的悬浮颗粒 | |
| B. | 高锰酸钾溶液和双氧水进行环境消毒时原理是相同的 | |
| C. | 雾霾中含有大量超标的主要物质是SO2 | |
| D. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
 物质A~F都是初中化学中的常见物质,其中物质A是一种酸,物质C是一种盐,它们有如图所示的转化关系.反应①为A+B=D+E,反应②为B+C=E+F
物质A~F都是初中化学中的常见物质,其中物质A是一种酸,物质C是一种盐,它们有如图所示的转化关系.反应①为A+B=D+E,反应②为B+C=E+F