题目内容
19.一定条件下,在密闭容器中充入1mol N2和3mol H2进行如下反应:N2(g)+3H2(g)?2NH3(g),当N2、H2、NH3的浓度不再改变时,下列说法正确的是( )| A. | N2、H2完全反应生成2mol NH3 | B. | N2、H2、NH3的浓度一定相等 | ||
| C. | 反应已达到化学平衡状态 | D. | 正、逆反应速率相等且等于零 |
分析 A、此反应N2(g)+3H2(g)?2NH3(g)是可逆反应,不可能完全转化;
B、平衡时N2、H2、NH3的浓度不变;
C、当N2、H2、NH3的浓度不再改变时,说明达平衡状态;
D、化学平衡状态是动态平衡.
解答 解:A、此反应N2(g)+3H2(g)?2NH3(g)是可逆反应,不可能完全转化,所以N2、H2完全反应生成 NH3小于2mol,故A错误;
B、平衡时N2、H2、NH3的浓度不变,但不一定相等,故B错误;
C、当N2、H2、NH3的浓度不再改变时,说明达平衡状态,故C正确;
D、化学平衡状态是动态平衡,速率不为0,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
9.在同温同压下,A容器中盛有H2,B容器中盛有NH3,它们所含的原子总数相等,则两容器中气体的密度之比为( )
| A. | 2:1 | B. | 1:2 | C. | 2:3 | D. | 2:17 |
10.设 N A代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 2.3 g 金属钠所含钠原子数目为0.2 N A | |
| B. | 2 g 氢气所含原子数目为2 N A | |
| C. | 17 g NH 3所含的分子数为2 N A | |
| D. | N A个O 2和 N A个H 2的所含原子数目比等于16:1 |
14.下列有关化学用语表示正确的是( )
| A. | 氢氧根离子的电子式  | |
| B. | 硫原子的结构示意图 | |
| C. | 一氯乙烷的结构式CH3CH2Cl | |
| D. | 中子数为146、质子数为92 的铀(U)原子${\;}_{92}^{146}$U |
4.铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
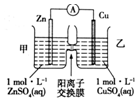

| A. | 锌电极上发生的反应: | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 电流由锌电极经电流表流向铜电极 | |
| D. | 电池工作一段时间后,乙池溶液的总质量增加 |
11.下列化学变化涉及的反应类型为加成反应的是( )
| A. | 苯→溴苯 | B. | 苯→硝基苯 | C. | 乙烯→氯乙烷 | D. | 乙醇→乙酸乙酯 |
8.类推法是一种非常重要的学习方法.下列类推中错误的是( )
| A. | 铁、铜等很多金属难溶于水,铅是一种金属,铅可能也难溶于水 | |
| B. | 铁能与盐酸发生置换反应,则铝与硝酸一定能发生置换反应 | |
| C. | SO2与CO2一样,与水反应生成酸性物质,则SO2也可能与NaOH溶液反应 | |
| D. | H2、CO、CH4气体燃烧前要进行验纯,其它可燃性气体与空气混合时也可能发生爆炸 |