题目内容
10.将200mL0.1mol/L的稀硫酸与300mL0.1mol/L的NaOH溶液混合后,能放出多少热量?如果溶液的密度为1g/mL,比热容按4.18kJ/(kg•℃)计算,这些热量能使混合液的温度升高多少度?(忽略溶液混合后的体积变化)分析 200mL0.1mol/L的稀硫酸的物质的量为n=CV=0.1mol/L×0.2L=0.02mol,300mL0.1mol/L的NaOH溶液的物质的量n=CV=0.1mol/L×0.3L=0.03mol,两者混合后,硫酸过量,生成水0.03mol,根据强酸强碱的中和热△H=-57.3KJ/mol,可以求出反应放出的热量Q.设温度的该变量为△T,然后根据Q=cm△T,即可求解.
解答 解:200mL0.1mol/L的稀硫酸的物质的量为n=CV=0.1mol/L×0.2L=0.02mol,300mL0.1mol/L的NaOH溶液的物质的量n=CV=0.1mol/L×0.3L=0.03mol,两者混合后,硫酸过量,生成水0.03mol,根据强酸强碱的中和热△H=-57.3KJ/mol,故可知反应放出的热量Q=57.3KJ/mol×0.03mol=1.719KJ.
设温度的该变量为△T,则Q=1.719KJ=cm△T=4.18kJ/(kg•℃)×(200mL+300mL)×1g/mL×10-3×△T,故可解得:△T=0.82℃.
答:反应后放出的热量为1.719KJ,能使混合溶液的温度升高0.82℃.
点评 本题考查了根据中和热进行的有关计算,应注意中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
20.某同学根据H2S和浓H2SO4的性质做出下列推测,其中正确的是( )
| A. | 浓H2SO4具有强氧化性是因为其中含+6价S,所有只要含最高价+6价S的化合物就具有强氧化性 | |
| B. | H2S中的S处于最低价,因此其不可能具有氧化性 | |
| C. | 浓H2SO4可把Na2SO3氧化 | |
| D. | 因为元素化合价变化以相邻价态之间转化最容易,因此发生氧化还原反应时,浓H2SO4对应的产物一般为SO2 |
1.25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.lmol•L-lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4-)>c(H2C2O4)>c(C2O42- ) | |
| B. | 0.lmol•L-1NaHS 溶液:C(OH-)+c(S2-)=c( H+)+c(H2S) | |
| C. | 0.lmol•L-1CH3COOH 溶液和 0.lmol•L-1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c( OH-) | |
| D. | 0.lmol•L-lNH4HSO4 溶液中滴加 0.lmol•L-1NaOH 溶液至中性:c(Na+ )>c(SO42- )>c(NH4+ )>c(OH-)=c(H+) |
5.下列说法不正确的是( )
| A. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,金属铝的熔点较低 | |
| B. | 铝与Fe2O3发生铝热反应后固体的质量不变 | |
| C. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | Al、HCl、NaOH中任意两种物质在一定条件下均能发生反应 |
1.某种直链饱和脂肪酸甘油酯22.25g,皂化时需3.00g NaOH,则与这种脂肪酸中的碳原子数接近的数值是( )
| A. | 15 | B. | 16 | C. | 17 | D. | 18 |
8.在允许加热的条件下,只用一种试剂就可以鉴别(NH4)2SO4、KCl、Al2(SO4)3和Fe2(SO4)34种溶液,这种试剂是( )
| A. | 氢氧化钠溶液 | B. | 氨水 | C. | 硝酸银溶液 | D. | 氯化钡溶液 |
5.下列说法不正确的是( )
①CH3-CH═CH2和CH2═CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2L的庚烷所含的分子数为0.5NA(NA为阿伏加德罗常数)
①CH3-CH═CH2和CH2═CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2L的庚烷所含的分子数为0.5NA(NA为阿伏加德罗常数)
| A. | ①⑤ | B. | ②③④ | C. | ③⑤ | D. | ④⑤ |
6.与50ml 0.2mol/L的Na2CO3溶液中Na+浓度相等的溶液是( )
| A. | 100ml 0.2mol/L的NaCl溶液 | B. | 50ml 0.1mol/L的Na2SO4溶液 | ||
| C. | 150ml 0.2mol/L的NaNO3溶液 | D. | 1000ml 0.2mol/L的Na2SO3溶液 |
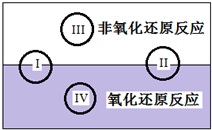 氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题:
氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题: