题目内容
5.下列说法不正确的是( )| A. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,金属铝的熔点较低 | |
| B. | 铝与Fe2O3发生铝热反应后固体的质量不变 | |
| C. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | Al、HCl、NaOH中任意两种物质在一定条件下均能发生反应 |
分析 铝为i活泼金属,可用于冶炼熔点较高的金属,即可与强酸反应,也可与强碱反应,铝与氧气反应生成熔点较高的氧化铝,以此解答该题.
解答 解:A.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,形成氧化膜,三氧化二铝的熔点高于铝的熔点,包住了熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落,故A错误;
B.化学反应遵循质量守恒定律,反应物、生成物都是固体,反应前后质量不变,故B正确;
C.铝于氢氧化钠溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,故C正确;
D.铝即可与强酸反应,也可与强碱反应,盐酸、氢氧化钠发生中和反应,故D正确.
故选A.
点评 本题多角度考查铝及其化合物的性质,为高频考点,侧重于双基的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
15.检验牙膏中是否含有甘油选用的试剂是( )
| A. | 氢氧化钠溶液 | B. | 氢氧化铜浊液 | C. | 醋酸溶液 | D. | 碳酸钠溶液 |
20.甲同学对Cl2与FeCl2和KSCN混合溶液的反应进行如下实验探究.请回答下列问题:
(1)装置B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)装置A中溶液变红的原因是2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3(用离子方程式表示).
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应.甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为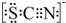
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取装置A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素(填名称).
③通过实验证明了SCN-中氮元素转化为NO3-,则SCN-与Cl2反应生成1mol CO2,转移电子的物质的量是16mol.
④(SCN)2的性质与卤素单质相似,并且还原性按Br-<SCN-<I-的混合溶液中,反应的离子方程式为(SCN)2+2I-=I2+2SCN-.
| 操作 | 现象 |
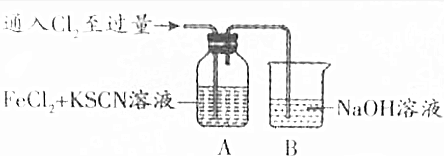 | Ⅰ.装置A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)装置A中溶液变红的原因是2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3(用离子方程式表示).
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应.甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
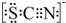
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②取装置A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素(填名称).
③通过实验证明了SCN-中氮元素转化为NO3-,则SCN-与Cl2反应生成1mol CO2,转移电子的物质的量是16mol.
④(SCN)2的性质与卤素单质相似,并且还原性按Br-<SCN-<I-的混合溶液中,反应的离子方程式为(SCN)2+2I-=I2+2SCN-.
1.胶体的最本质的特征是( )
| A. | 丁达尔效应 | |
| B. | 分散质颗粒的直径在1nm~100nm之间 | |
| C. | 布朗运动 | |
| D. | 可以通过滤纸 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.