��Ŀ����
7����ѧ������������������ɳ�����չ������أ������й�˵����ȷ���ǣ�������| A�� | MgO��Al2O3�ڹ�ҵ�������������²��ϣ�Ҳ�����ڵ�ⷨұ��Mg��Al | |
| B�� | ˮ��ұ���ø�ѹ���ȥ�����̳��������˽�������� | |
| C�� | ҽ�����õġ����͡���ɷ���̼�ᱵ��Ư�۵ijɷ�Ϊ������� | |
| D�� | ����ˮ���������Խ������ˮ��ӦΣ��������ˮ�м��뾻ˮ����������ʹ��ˮ���� |
���� A������þ�۵�ߣ���ҵ���õ���Ȼ�þ����ұ��þ��
B�����ݽ���ĵ�Ӿ�����ʽ��
C��̼�ᱵ�ܹ������ᷴӦ���ɿ������Ȼ�����
D����ˮ�м��뾻ˮ������ֻ�ܳ�ȥ���������ʣ�
��� �⣺A��MgO��Al2O3���߾��нϸߵ��۷е㣬�ڹ�ҵ�������������²��ϣ���ҵ���õ���������ķ�����ȡ�����õ���Ȼ�þ�ķ�����ȡþ����A����
B��ˮ��ұ���ø�ѹ���ȥ�����̳��������˽����Ӿ�����ʣ���B��ȷ��
C��̼�ᱵ�ܹ������ᷴӦ���ɿ������Ȼ���������ؽ����ж�����C����
D����ˮ�м��뾻ˮ������ֻ�ܳ�ȥ���������ʣ����ܼ����εĺ���������ʹ��ˮ��������D����
�ʴ�Ϊ��B��
���� ����Ϊ�����⣬�����˻�ѧ��ѧ���ص㡢��������Ⱦ�������������г����IJ��Ϻ�ʳƷ���Ӽ�����Ŀ�ѶȲ�������������Ӵ�������ע�����֪ʶ�Ļ��ۣ�

��ϰ��ϵ�д�
�����Ŀ
18���������ȣ�C1NO�����л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO��g��+C12��g��?2C1NO��g����
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��2NO2��g��+NaC1��s��?NaNO3��s��+ClNO��g�� K1
��4NO2��g��+2NaC1��s��?2NaNO3��s��+2NO��g��+Cl2��g�� K2
��2NO��g��+C12��g��?2C1NO��g�� K3
��K1��K2��K3֮��Ĺ�ϵΪK3=$\frac{{{K}^{2}}_{1}}{{K}_{2}}$��
��2����֪���ֻ�ѧ���ļ����������±����������ȵĽṹΪCl-N=O����
��2NO��g��+C12��g��?2C1NO��g����Ӧ�ġ�H��a�Ĺ�ϵΪ��H=289-2akJ/mol��
��3����1L�ĺ����ܱ������г���2molNO��g����1molC12��g�����ڲ�ͬ�¶��²��c��C1NO����ʱ��Ĺ�ϵ��ͼA��

����ͼA���ж�T1��T2���÷�Ӧ�ġ�H��0 ���������������=������
�ڷ�Ӧ��ʼ��10minʱNO��ƽ����Ӧ����v��NO��=0.1mol/��L•min����
��T2ʱ�÷�Ӧ��ƽ�ⳣ��K=2��
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO��g����Cl2��g����ƽ��ʱClNO�����������$\frac{n��NO��}{n��C{1}_{2}��}$�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת����������A�㣮
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��2NO2��g��+NaC1��s��?NaNO3��s��+ClNO��g�� K1
��4NO2��g��+2NaC1��s��?2NaNO3��s��+2NO��g��+Cl2��g�� K2
��2NO��g��+C12��g��?2C1NO��g�� K3
��K1��K2��K3֮��Ĺ�ϵΪK3=$\frac{{{K}^{2}}_{1}}{{K}_{2}}$��
��2����֪���ֻ�ѧ���ļ����������±����������ȵĽṹΪCl-N=O����
| ��ѧ�� | N��O | Cl-Cl | Cl-N | N=O |
| ����/kJ��mol-1 | 630 | 243 | a | 607 |
��3����1L�ĺ����ܱ������г���2molNO��g����1molC12��g�����ڲ�ͬ�¶��²��c��C1NO����ʱ��Ĺ�ϵ��ͼA��

����ͼA���ж�T1��T2���÷�Ӧ�ġ�H��0 ���������������=������
�ڷ�Ӧ��ʼ��10minʱNO��ƽ����Ӧ����v��NO��=0.1mol/��L•min����
��T2ʱ�÷�Ӧ��ƽ�ⳣ��K=2��
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO��g����Cl2��g����ƽ��ʱClNO�����������$\frac{n��NO��}{n��C{1}_{2}��}$�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת����������A�㣮
15��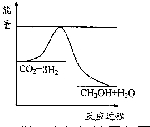 ��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú������
��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú������
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ/mol
�ٸ÷�Ӧ�ڸ��������Է����е�ԭ���ǡ�S��0
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����BDF������ĸ����ͬ����
A�������е�ѹǿ���� B��1mol H-H �����ѵ�ͬʱ����2mol H-O ��
C��V ��CO��=V ��H2��D���ܱ��������ݻ����ٸı�
E������1mol ˮ��ͬʱ����1mol H2 F���������ܶȲ���
�۸÷�Ӧ��ƽ�ⳣ���ı���ʽK=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$��
��2��ˮú���ٽ�һ����Ӧ����ȡ��������ӦΪH2O��g��+CO��g��?H2��g��+CO2��g����ij�¶��¸÷�Ӧ���淴Ӧƽ�ⳣ��K=$\frac{4}{9}$�����¶����ڼס��ҡ������������ܱ������У�ֻͶ��H2��g����CO2��g��������ʼŨ�����±���ʾ�������жϲ���ȷ����B��
A����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
B��ƽ��ʱ�����кͱ���H2��ת���ʲ���
C��ƽ��ʱ������c��CO2���Ǽ��е�2 ��
D��ƽ��ʱ������CO2��ת���ʴ���60%
��3��Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ•mol-1���ı仯�������Ϊ1L �ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc ��CH3OH����С����A��
A�������¶� ��
B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з������
D���ٳ���1mol CO2 ��3mol H2��
 ��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú������
��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú��������1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ/mol
�ٸ÷�Ӧ�ڸ��������Է����е�ԭ���ǡ�S��0
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����BDF������ĸ����ͬ����
A�������е�ѹǿ���� B��1mol H-H �����ѵ�ͬʱ����2mol H-O ��
C��V ��CO��=V ��H2��D���ܱ��������ݻ����ٸı�
E������1mol ˮ��ͬʱ����1mol H2 F���������ܶȲ���
�۸÷�Ӧ��ƽ�ⳣ���ı���ʽK=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$��
��2��ˮú���ٽ�һ����Ӧ����ȡ��������ӦΪH2O��g��+CO��g��?H2��g��+CO2��g����ij�¶��¸÷�Ӧ���淴Ӧƽ�ⳣ��K=$\frac{4}{9}$�����¶����ڼס��ҡ������������ܱ������У�ֻͶ��H2��g����CO2��g��������ʼŨ�����±���ʾ�������жϲ���ȷ����B��
| ��ʼ Ũ�� | �� | �� | �� |
| c��H2��/mol/L | 0.010 | 0.020 | 0.020 |
| c��CO2��/mol/L | 0.010 | 0.010 | 0.020 |
B��ƽ��ʱ�����кͱ���H2��ת���ʲ���
C��ƽ��ʱ������c��CO2���Ǽ��е�2 ��
D��ƽ��ʱ������CO2��ת���ʴ���60%
��3��Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ•mol-1���ı仯�������Ϊ1L �ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc ��CH3OH����С����A��
A�������¶� ��
B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з������
D���ٳ���1mol CO2 ��3mol H2��
2������˵�����ʾ������ȷ���ǣ�������
| A�� | �����ʵ������������������ֱ���ȫȼ�գ����߷ų��������� | |
| B�� | ��ϡ��Һ�У�H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ/mol��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��ų����ȴ���57.3kJ | |
| C�� | ��C��s��ʯī��=C��s�����ʯ����H=+1.90kJ/mol��֪��ʯīû�н��ʯ�ȶ� | |
| D�� | ��101kPaʱ��2g��������ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g��=2H2O��l����H=-285.8kJ/mol |
12����CuO+H2 $\frac{\underline{\;����\;}}{\;}$Cu+H2O��Ӧ�У�����˵����ȷ���ǣ�������
| A�� | CuO�ǻ�ԭ���������� | |
| B�� | H2�ǻ�ԭ���������� | |
| C�� | H2O�Ȳ�����������Ҳ���ǻ�ԭ���� | |
| D�� | Cu�ǻ�ԭ�������ԭ |
19�����й����Ƽ��仯�����˵��������ǣ�������
| A�� | �ơ��������ơ��������ơ�̼��������ʱ����ʻ�ɫ | |
| B�� | �п��Ľ����Ʊ�¶�ڿ����У������ı���䰵����2Na+O2�TNa2O2��Ӧ | |
| C�� | �������ƿ�����������ߺ�DZˮͧ������������Դ | |
| D�� | ��������Ͷ������ͭ��Һ�ɲ���������ͭ���������� |
16�����з��뷽���в���ȷ���ǣ�������
| A�� | ������ȡ���������Ȼ�̼��ȡ��ˮ�е��嵥�� | |
| B�� | ��������ķ������Է���е����ϴ��Һ������ | |
| C�� | ���÷�Һ�ķ�������ƾ���ˮ | |
| D�� | ���ýᾧ�ķ�����ȥKNO3�е��Ȼ��� |
17��25��ʱ�����и���������ָ����Һ��һ���ܴ���������ǣ�������
| A�� | ��ɫ��Һ�У�K+��Na+��Cu2+��SO42- | |
| B�� | Kw/c��OH-��=10-12 mol•L-1����Һ��Na+��K+��SiO32-��Cl- | |
| C�� | 0.1 mol•L-1FeSO4��Һ�У�K+��NH4+��MnO4-��ClO- | |
| D�� | ʹ��̪���ɫ����Һ��Na+��Ba2+��NO3-��Cl- |