题目内容
2.下列化学用语正确的是( )| A. | 8个质子10个中子的核素符号:10Ar | B. | H2O的电子式: | ||
| C. | 四氯化碳的电子式: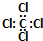 | D. | S2-离子的结构示意图: |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
B.水为共价化合物,不能标出所带电荷;
C.四氯化碳的电子式中漏掉了氯原子的3对孤电子对;
D.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构.
解答 解:A.8个质子10个中子的核素为O元素,其质量数为18,该核素正确的表示方法为818O,故A错误;
B.水分子属于共价化合物,不存在阴阳离子,正确的电子式为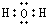 ,故B错误;
,故B错误;
C.四氯化碳属于共价化合物,碳原子和氯原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为: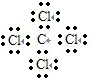 ,故C错误;
,故C错误;
D.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子离子的结构示意图为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握电子式、离子结构示意图、元素符号等化学用语的表示方法,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18gH20中含NA个质子 | |
| B. | 1L 1mol•L一1的CuSO4溶液中含NA个Cu2+ | |
| C. | 常温常压下,2.24L Cl2中含0.2NA个氯原子 | |
| D. | 0.5mol Al与足量NaOH溶液充分反应,转移的电子数目为1.5NA |
13.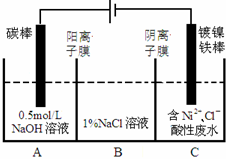 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)( )
 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)( )
| A. | 碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O | |
| B. | 为了提高Ni的产率,电解过程中需要控制废水pH | |
| C. | 电解过程中,B中NaCl溶液的物质的量浓度将不断减小 | |
| D. | 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
10.下列物质中,既能发生消去反应生成烯烃,又能发生氧化反应生成醛的是( )
| A. | 2-甲基-1-丁醇 | B. | 2,2-二甲基-1-丁醇 | ||
| C. | 2-甲基-2-丁醇 | D. | 2,3-二甲基-2-丁醇 |
17.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术.已知反应:Fe2O3+3Na2O2=2Na2FeO4+Na2O,下列说法正确的是( )
| A. | Na2O2既是氧化剂又是还原剂 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 3molNa2O2发生反应,有12mol电子转移 | |
| D. | Na2FeO4在水中被氧化得到Fe3+,Fe3+水解生成氢氧化铁,可净水 |
7.甲烷在高温下可分解生成C2H2和H2.一定量的甲烷部分分解成C2H2和H2后,仍有CH4剩余,所得混合物的平均式量为12.8,则甲烷的分解率为( )
| A. | 10% | B. | 25% | C. | 50% | D. | 75% |
11.下列说法正确的是( )
| A. | 某有机物的结构简式为: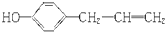 ,按官能团分,既可属于醇类,也可属于烯烃类 ,按官能团分,既可属于醇类,也可属于烯烃类 | |
| B. |  的名称为2-甲基-3-丁烯 的名称为2-甲基-3-丁烯 | |
| C. | 用分液的方法分离乙酸和乙酸乙酯 | |
| D. | 用重结晶的方法提纯苯甲酸 |
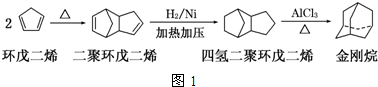
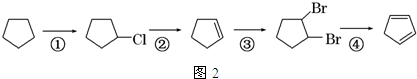
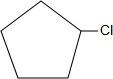 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$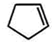 +NaCl+H2O;反应的化学方程式:
+NaCl+H2O;反应的化学方程式: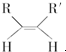 $\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO,请写出下列反应产物的结构简式:
$\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO,请写出下列反应产物的结构简式: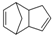 $\stackrel{O3}{→}$$\stackrel{H_{2}O/Zn}{→}$
$\stackrel{O3}{→}$$\stackrel{H_{2}O/Zn}{→}$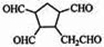 ;
;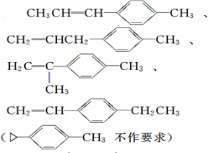 .
.