题目内容
5.从下列提供的试剂和操作中选择最佳组合完成从碘水中提取单质碘( )①酒精 ②苯 ③四氯化碳 ④分液 ⑤萃取 ⑥蒸馏.
| A. | ②④ | B. | ②④⑤ | C. | ②④⑤⑥ | D. | ③④⑤⑥ |
分析 因碘不易溶于水,易溶于有机溶剂,则从碘水中提取单质碘,选择不溶于水的有机溶剂、萃取后分液、蒸馏得到碘,以此来解答.
解答 解:因碘不易溶于水,易溶于有机溶剂,则从碘水中提取单质碘,选择不溶于水的有机溶剂,则②③均可,不能选择①,因酒精与水互溶;
然后选⑤,再④,最后选⑥分离出碘,即组合为③④⑤⑥或②④⑤⑥,
故选CD.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯方法、实验技能为解答的关键,侧重分析与实验能力的考查,注意萃取剂的选择,题目难度不大.

练习册系列答案
相关题目
8.下列溶液中的c(Cl-)与50mL 1mol•L-1氯化铝溶液中的c(Cl-)相等的是( )
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 75 mL 2 mol•L-1氯化铵溶液 | ||
| C. | 150 mL 1 mol•L-1氯化钾溶液 | D. | 75 mL 1 mol•L-1氯化铝溶液 |
13.少量铁粉与100mL 0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦改用10mL 0.1mol/L盐酸.
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦改用10mL 0.1mol/L盐酸.
| A. | ①②⑥⑦ | B. | ③⑥⑦ | C. | ③⑦ | D. | ④⑤⑦ |
20.一定条件下,在密闭容器中进行如下反应:NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 增大压强同时充入NO |
17.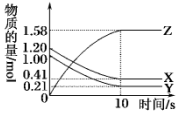 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用X表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10 s,Y的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应10s时达到化学平衡状态,Z的平衡浓度为0.79 mol•L-1 | |
| D. | 反应的化学方程式为2X(g)+2Y(g)?Z(g) |
14.下列各组离子,在指定环境中一定能大量共存的是( )
| A. | pH=7的溶液中:Al3+、K+、SO42-、HCO3- | |
| B. | FeCl2溶液中:SO42-、H+、MnO4-、Na+ | |
| C. | 水电离的c (H+)=1×10-13 mol•L-1:S2-、SO32-、S2O32-、SO42- | |
| D. | 滴加甲基橙试剂显红色的溶液中:Na+、NH4+、Cl-、NO3- |
15.在恒温恒容的容器中,发生反应:H2(g)+CO(g)?C(s)+H2O(g).初始时加入平均相对分子质量为15的H2、CO混合气,一段时间后测得气体的平均相对分子质量为16,下列说法中不正确的是( )
| A. | 反应前后气体的压强之比为4:3 | |
| B. | 反应前后气体的密度之比为l5:16 | |
| C. | H2与CO的转化率相等,均为50% | |
| D. | 若H2与CO按8:5体积比混合,则反应前后混合气体的平均相对分子质量不变 |
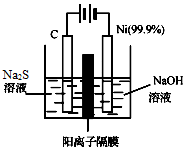 硫及其化合物广泛分布于自然界中,硫酸工业在国民经济中占有极其重要的地位,运用相关原理回答下列问题:
硫及其化合物广泛分布于自然界中,硫酸工业在国民经济中占有极其重要的地位,运用相关原理回答下列问题: