题目内容
3.已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | ||||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | 放出热量:32.8kJ | |
| A. | 容器①中反应达平衡时,CO的转化率为80% | |
| B. | 平衡时,两容器中CO2的浓度相等 | |
| C. | 容器①中CO的转化率等于容器②中CO2的转化率 | |
| D. | 容器①中CO反应速率等于H2O(g)的反应速率 |
分析 A.根据平衡时放出的热量,结合热化学方程式计算参加反应的CO的物质的量,再根据转化率定义计算;
B.容器①②温度相同,同一可逆反应正逆平衡常数互为倒数,根据容器①计算平衡常数,令容器②中CO2的物质的量变化量为amol,表示出平衡时各组分的物质的量,反应前后气体的体积不变,利用物质的量代替浓度代入平衡常数表达式计算a的值,进而计算CO2的浓度,
C.根据B中的计算判断;
D.速率之比等于化学计量数之比.
解答 解:A.平衡时放出的热量为32.8 kJ,故参加反应的CO的物质的量$\frac{32.8\;kJ}{41kJ}$×1mol=0.8mol,CO的转化率为$\frac{0.8mol}{1mol}$×100%=80%,故A正确;
B.容器①②温度相同,平衡常数相同,根据容器①计算平衡常数,由A计算可知,平衡时CO的物质的量变化量为0.8mol,
则:CO(g)+H2O(g)?CO2(g)+H2(g)
开始(mol):1 4 0 0
变化(mol):0.8 0.8 0.8 0.8
平衡(mol):0.2 3.2 0.8 0.8
故平衡常数K=$\frac{0.8×0.8}{0.2×3.2}$=1,
故容器②中的平衡常数为1,令容器②中CO2的物质的量变化量为amol,则:
CO2(g)+H2(g)?CO(g)+H2O(g)
开始(mol):1 4 0 0
变化(mol):a a a a
平衡(mol):1-a 4-a a a
所以$\frac{a×a}{(1-a)×(4-a)}$,解得a=0.8,
由A中计算可知容器①平衡时CO2的物质的量为0.8mol,容器②中CO2的物质的量为1mol-0.8mol=0.2mol,容器的体积相同,平衡时,两容器中CO2的浓度不相等,故B错误;
C.→B计算可知CO2的转化率为$\frac{0.8mol}{1mol}$×100%=80%,故C正确;
D.速率之比等于化学计量数之比,故容器①中CO反应速率等于H2O的反应速率,故D正确;
故选B.
点评 本题考查化学平衡的计算,为高考常见题型,题目难度中等,平衡判断和平衡常数的计算是解题关键,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

 阅读快车系列答案
阅读快车系列答案| A. | NaOH溶液中滴入CuSO4溶液 OH-+Cu2+=Cu(OH)2↓ | |
| B. | 乙醛发生银镜反应CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$CH3COO-+NH4+2Ag↓+3NH3+H2O | |
| C. | 醋酸与碳酸钠溶液反应 CO32-+2H+=H2O+CO2↑ | |
| D. | 溴乙烷中滴入AgNO3溶液 Ag++Br-=AgBr↓ |
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 氯化铁溶液 | 氯化亚铁 | 过量铁粉 | 过滤 |
| B | 二氧化碳 | 二氧化硫 | 饱和NaHCO3溶液 | 洗气 |
| C | 二氧化硅 | 氧化铝 | 氨水 | 过滤 |
| D | 氯化钠溶液 | 碘化钠 | 四氯化碳 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
 己二酸
己二酸 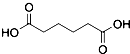 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图:3
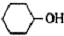 +8HNO3→3
+8HNO3→3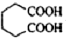 +8NO↑+7H2O
+8NO↑+7H2O可能用到的有关数据如表:
| 物资 | 密度(20℃) | 熔点 | 沸点 | 溶解性 | 相对分子质量 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度3.6g,可混溶于乙醇、苯 | 100 |
| 己二酸 | 1.36g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇,不溶于苯. | 146 |
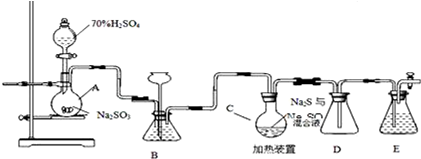
I、在三口烧瓶中加入16mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.
III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品.
V、粗产品经提纯后称重为5.7g.
请回答下列问题:
(1)仪器b的名称为球形冷凝管(或冷凝管).
(2)向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则.可能造成较严重的后果,试列举一条可能产生的后果:
反应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的NO2气体来不及被碱液吸收而外逸到空气中.
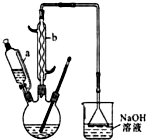
(3)已知用NaOH溶液吸收尾气时发生的相关反应方程式为:
2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH=2NaNO2+H2O;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:
2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO+NO2+Na2CO3=2NaNO2+CO2.
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和苯洗涤晶体.
(5)粗产品可用重结晶 法提纯(填实验操作名称).本实验所得到的己二酸产率为75%.
 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2•6C2H5OH.
已知乙醇可以和氯化钙反应生成微溶于水的CaCl2•6C2H5OH.