题目内容
19.下列试剂中,能较简便地将溶液中的Mg2+、Al3+分离的是( )| A. | NaOH溶液 | B. | 氨水 | C. | 硝酸 | D. | 硫酸 |
分析 Mg2+、Al3+均与NaOH反应,分别转化为沉淀、偏铝酸根离子,过滤可分离,沉淀、滤液均与足量酸反应可得到Mg2+、Al3+,以此来解答.
解答 解:A.与NaOH反应,分别转化为沉淀、偏铝酸根离子,过滤可分离,沉淀、滤液均与足量酸反应可得到Mg2+、Al3+,故A选;
B.二者均与氨水反应生成沉淀,不能分离,故B不选;
C.二者均与硝酸不反应,不能分离,故C不选;
D.二者均与硫酸不反应,不能分离,故D不选;
故选A.
点评 本题考查混合物分离实验设计,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 将25 g CuSO4•5H2O溶于100 mL蒸馏水中,可以配成100 mL 1.0 mol/L CuSO4溶液 | |
| B. | 可以用重结晶法除去KNO3固体中混杂的NaCl,这是因为NaCl在水中的溶解度很大 | |
| C. | 利用实验器材(规格和数量不限):烧杯、玻璃棒、胶头滴管、分液漏斗,能完成用溴水和CCl4除去NaBr溶液中的少量NaI的实验 | |
| D. | 用润湿的pH试纸测稀酸溶液的pH,测定值偏小 |
10.下列有关盐类水解的说法中,不正确的是( )
| A. | NaHCO3属于酸式盐,其水溶液显酸性 | |
| B. | CuCl2水解的实质是Cu2+与水电离出来的OH-结合生成了弱电解质Cu(OH)2 | |
| C. | 利用纯碱水解显碱性,可除去物品表面的油污 | |
| D. | 明矾【KAl(SO4)2•12H2O】用于净水的原因是明矾电离产生的Al3+水解产生Al(OH)3胶体,Al(OH)3胶体吸附水中悬浮的杂质. |
4.已知位于同周期的X、Y、Z三种主族元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,下列判断不正确的是( )
| A. | 元素的非金属性:X>Y>Z | |
| B. | 在元素周期表中它们依次处于第ⅦA族、第ⅥA族、第ⅤA族 | |
| C. | 酸性:H3ZO4>H2YO4>HXO4 | |
| D. | 气态氢化物的稳定性:HX>H2Y>ZH3 |
11.糖类是由C、H、O三种元素组成的一类有机化合物.下列物质不属于糖类的是( )
| A. | 葡萄糖 | B. | 淀粉 | ||
| C. | 纤维素 | D. | 味精(主要成分谷氨酸钠) |
8.某有机物结构简式为: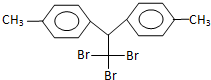 ,有关它的说法正确的是( )
,有关它的说法正确的是( )
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子式为C16H14Br3 | ||
| C. | 分子中最多有24个原子共面 | D. | 1mol该物质能与6mol H2加成 |
9.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1 Na2S溶液中一定有:c(OH-)=c(H+)+c(HS-)+2c(H2S) | |
| B. | 向NH4Cl溶液中加入适量氨水,得到的碱性混合溶液中一定有:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 加热Na2S溶液,溶液c(OH-)肯定增大,c(H+)肯定减小 | |
| D. | 加水稀释0.1mol•L-1醋酸溶液,电离平衡向右移动,c(H+)一定减小 |