题目内容
4.已知位于同周期的X、Y、Z三种主族元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,下列判断不正确的是( )| A. | 元素的非金属性:X>Y>Z | |
| B. | 在元素周期表中它们依次处于第ⅦA族、第ⅥA族、第ⅤA族 | |
| C. | 酸性:H3ZO4>H2YO4>HXO4 | |
| D. | 气态氢化物的稳定性:HX>H2Y>ZH3 |
分析 同周期的X、Y、Z三种主族元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,可知X、Y、Z的最高正化合价分别为+7、+6、+5,分别处于第ⅦA族、第ⅥA族、第ⅤA族,同周期自左而右金属性增强,最高价氧化物对应水化物的酸性最强、氢化物稳定性增强.
解答 解:A.同周期的X、Y、Z三种主族元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,可知X、Y、Z的最高正化合价分别为+7、+6、+5,分别处于第ⅦA族、第ⅥA族、第ⅤA族,同周期自左而右金属性增强,则元素的非金属性:X>Y>Z,故A正确;
B.X、Y、Z的最高正化合价分别为+7、+6、+5,分别处于第ⅦA族、第ⅥA族、第ⅤA族,故B正确;
C.元素的非金属性:X>Y>Z,故最高价氧化物的水化物酸性:HXO4>H2YO4>H3ZO4,故C错误;
D.X、Y、Z的最高正化合价分别为+7、+6、+5,对应的氢化物为HX、H2Y、ZH3,元素的非金属性:X>Y>Z,则气态氢化物的稳定性:HX>H2Y>ZH3,故D正确.
故选:C.
点评 本题涉及元素周期律知识,旨在考查学生对基础知识的理解掌握与简单应用,熟练注意元素周期律,掌握金属性、非金属性强弱比较方法.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
14.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 16g O2一定条件下与一定量的钠反应转移的电子数一定为2NA | |
| B. | 14 g乙烯和丙烯的混合气体中总原子数为3NA | |
| C. | 1L1 mol/L饱和FeCl3溶液滴入沸水中完全水解生成NA个氢氧化铁胶体粒子 | |
| D. | 0.1 mol•L-1 氢氧化钠溶液中所含钠离子数为0.1NA |
15.下列离子方程式正确的是( )
| A. | NaHCO3溶液和过量NaOH溶液混合HCO3-+OH-=CO32-+H2O | |
| B. | 在氢氧化钠溶液中滴加少量氯化铝 Al3++3OH-=Al(OH)3↓ | |
| C. | 将少量稀盐酸滴加到碳酸钠溶液中:2H++CO32-=H2O+CO2↑ | |
| D. | 向硫酸铝钾溶液中滴加氢氧化钡溶液至沉淀物质的量最多3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
12.X、Y是短周期元素,它们可组成化合物XY,下列说法中,正确的是( )
| A. | 若Y的原子序数为m,X的原子序数一定是m±6 | |
| B. | X、Y可以属于同一周期,也可以属于不同周期 | |
| C. | X与Y一定不属于同一主族 | |
| D. | XY一定是离子化合物 |
19.下列试剂中,能较简便地将溶液中的Mg2+、Al3+分离的是( )
| A. | NaOH溶液 | B. | 氨水 | C. | 硝酸 | D. | 硫酸 |
9.短周期元素A、B、C、D、E 的原子序数依次递增,A原子最外层电子数是次外层电子数的2 倍,C 的氢化物在常温下为液体,C 和D 的化合物可以制造高性能通讯材料,E 元素的最高化合价和最低化合价的代数和为6.下列叙述错误的是( )
| A. | E 元素处于元素周期表中第3 周期第ⅦA 族 | |
| B. | 元素A、B、C 的原子半径:C>B>A | |
| C. | 元素B、C、D 的非金属性:C>B>D | |
| D. | 一定条件下,A 单质可以将D 单质从其氧化物中置换出来 |
14.下列物质中,有1种与另外3种颜色不同,该物质是( )
| A. | 氢氧化钠 | B. | 碳酸钠 | C. | 氧化钠 | D. | 过氧化钠 |


 .
. .
.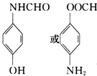 .
. 的合成路线补充完整.
的合成路线补充完整.
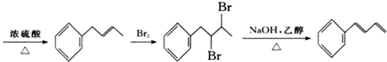 (无机试剂及溶剂任选).
(无机试剂及溶剂任选).