题目内容
1.元素性质的周期性变化不包括( )| A. | 原子半径 | B. | 元素的主要化合价 | ||
| C. | 相对原子质量 | D. | 金属性和非金属性 |
分析 随着原子序数的递增,核外电子排布、元素的化合价、原子半径、金属性和非金属性呈现周期性变化.
解答 解:随着原子序数的递增,核外电子排布、元素的化合价、原子半径、金属性和非金属性呈现周期性变化,但由于相对原子质量的决定因素是原子中质子数、中子数及同一元素的同位素原子在自然界中的物质的量分数,所以相对原子质量不呈周期性变化.
故选C.
点评 本题考查随着原子序数的递增,元素性质的变化,要理解元素性质呈周期性变化的原因是元素原子的核外电子排布的周期性变化的结果.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
11.科学家发现C60后,近年又合成了许多球形富勒烯分子,如C70等,下列对C70说法正确的是( )
| A. | 它与金刚石互为同素异形体 | |
| B. | 它与C60互称同分异构体 | |
| C. | 它与C60的物理性质与化学性质完全相同 | |
| D. | 它与13C互为同位素 |
9.在平衡体系N2+O2?2NO-Q中,能使氮的转化率提高的措施是( )
| A. | 通入N2 | B. | 加压 | ||
| C. | 升高温度 | D. | 使用合适的催化剂 |
13.满足分子式为C4H8ClBr的有机物共有( )
| A. | 11种 | B. | 12种 | C. | 13种 | D. | 14种 |
11.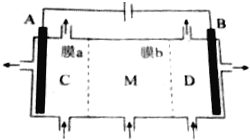 离子交换膜在电解池和原电池中有着独特的作用.利用离子交换膜技术,通过如图所示装置电解Na2SO3溶液制取NaOH溶液和H2SO4溶液(其中A、B电极为惰性电极).下列说法正确的是( )
离子交换膜在电解池和原电池中有着独特的作用.利用离子交换膜技术,通过如图所示装置电解Na2SO3溶液制取NaOH溶液和H2SO4溶液(其中A、B电极为惰性电极).下列说法正确的是( )
 离子交换膜在电解池和原电池中有着独特的作用.利用离子交换膜技术,通过如图所示装置电解Na2SO3溶液制取NaOH溶液和H2SO4溶液(其中A、B电极为惰性电极).下列说法正确的是( )
离子交换膜在电解池和原电池中有着独特的作用.利用离子交换膜技术,通过如图所示装置电解Na2SO3溶液制取NaOH溶液和H2SO4溶液(其中A、B电极为惰性电极).下列说法正确的是( )| A. | a膜为阳离子交换膜 | |
| B. | 溶液中SO${\;}_{3}^{2-}$由M室经b膜移向D室 | |
| C. | A极的电极反应式为SO${\;}_{3}^{2-}$+2e-+H2O═SO${\;}_{4}^{2-}$+2H+ | |
| D. | C室溶液呈酸性,M室溶液呈中性,D室溶液呈碱性 |
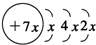 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: ,这样排布遵循了泡利原理和洪特规则.
,这样排布遵循了泡利原理和洪特规则. .
.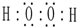 ;肼的结构式
;肼的结构式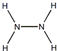 ;
;