题目内容
15.第3周期某元素的原子,其最外层3p亚层上有一个未成对电子,则关于该元素的描述正确的是( )| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
分析 第3周期元素的原子,其最外层3p能级上仅有一个未成对电子,价层电子排布为3s23p1或3s23p5,为Al元素或Cl元素,以此解答该题.
解答 解:第3周期元素的原子,其最外层3p能级上仅有一个未成对电子,价层电子排布为3s23p1或3s23p5,为Al元素或Cl元素,
A.如为Al,则元素最高价氧化物的水化物为弱碱,故A错误;
B.如为Al,则为固体,故B错误;
C.为Al或Cl元素,元素的最高价氧化物水化物为氢氧化铝或高氯酸,二者都可与氢氧化钠反应,故C正确;
D.Al原子半径在第三周期中不是最小,故D错误.
故选C.
点评 本题考查结构性质位置关系,为常见题型,侧重于学生的分析能力的考查,难度不大,掌握核外电子排布规律判断元素是解题的关键,注意把握原子结构的特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.关于氧气(O2)和臭氧(O3)说法正确的是( )
| A. | 互为同素异形体 | |
| B. | 二者相互转化是物理变化 | |
| C. | 同温同压下,等体积的氧气和臭氧含有相同的分子数 | |
| D. | 等物质的量的氧气和臭氧含有相同的质子数 |
6.下列关于各图的叙述,正确的是( )
| A. | 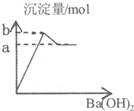 图表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀的量关系曲线 | |
| B. | 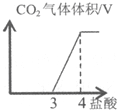 图表示向含有等物质的量的NaOH和Na2CO3溶液中加入盐酸放出CO2的关系曲线 | |
| C. | 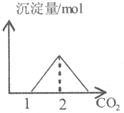 图表示向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2的产生沉淀关系曲线 | |
| D. |  图表示向NaOH溶液中滴加AlCl3溶液产生沉淀的量关系曲线 |
3.下列化学用语表示正确的是( )
| A. | 葡萄糖的最简式(实验式):CH2O | B. | 乙烯的结构简式为:CH2CH2 | ||
| C. | 氮气的电子式: | D. | 核内有8个中子的碳原子:86C |
10.下列物质由CH2═CH-CH2-CH3与Br2加成得到的是( )
| A. | CH3CH2CHBrCH2Br | B. | CH3CHBrCHBrCH3 | C. | 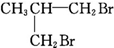 | D. | 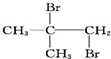 |
20.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-的数目为0.02NA | |
| B. | 标准状况下,11.2 L乙醇所含的羟基数为0.5NA | |
| C. | 1 mol Fe与1 mol Cl2反应转移电子数一定为3NA | |
| D. | 常温常压下,19g H3O+含有10NA个电子 |
7.化学实验是化学学科学习、探究的基础.
(1)下列描述错误的是acde.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:CO32-、Br-、Na+、SO32-
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:
V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
(1)下列描述错误的是acde.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:CO32-、Br-、Na+、SO32-
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
5.下列状态的物质,既能导电又属于电解质的是( )
| A. | MgCl2晶体 | B. | NaCl溶液 | C. | 液态HCl | D. | 熔融的NaOH |