题目内容
5.下列状态的物质,既能导电又属于电解质的是( )| A. | MgCl2晶体 | B. | NaCl溶液 | C. | 液态HCl | D. | 熔融的NaOH |
分析 电解质是水溶液中或熔融状态下都导电的化合物,物质导电的条件:存在自由电子或者自由移动的离子,据此解答.
解答 解:A.MgCl2晶体是电解质但不能导电,故A错误;
B.虽然氯化钠溶液能导电,但氯化钠溶液是混合物不是化合物,故B错误;
C.液态氯化氢是电解质但不能导电,故C错误;
D.熔融的氢氧化钠是能导电的电解质,故D正确.
故选D.
点评 本题考查了电解质的概念,难度不大,注意电解质不一定导电,导电的物质不一定是电解质.

练习册系列答案
相关题目
15.第3周期某元素的原子,其最外层3p亚层上有一个未成对电子,则关于该元素的描述正确的是( )
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
16.工业上需要利用一批回收的含铜废料制造胆矾(CuSO4•5H2O).该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质.工艺流程为:
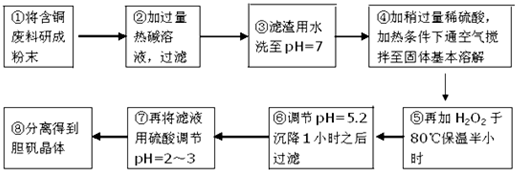
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如表:
请回答下列问题:
(1)步骤①中为什么要将含铜废料研磨成粉状?增大固体反应物的表面积,增大化学反应的速率.
(2)步骤②中的离子方程式(写出2个即可):2Al+2OH-+2H2O=2AlO2-+3H2↑、Si+2OH-+H2O=SiO32-+2H2↑或Al2O3+2OH-=2AlO2-+H2O或SiO2+2OH-=SiO32-+H2O.
(3)步骤⑤中H2O2参加反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)步骤⑥中调节溶液pH时适宜的物质是C、D(填序号).
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
(5)步骤⑦中用硫酸调节pH=2~3的原因是抑制Cu2+的水解,也不会引入杂质.
(6)步骤⑧的分离方法步骤是蒸发浓缩,冷却结晶,过滤,(洗涤、干燥).

部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
(1)步骤①中为什么要将含铜废料研磨成粉状?增大固体反应物的表面积,增大化学反应的速率.
(2)步骤②中的离子方程式(写出2个即可):2Al+2OH-+2H2O=2AlO2-+3H2↑、Si+2OH-+H2O=SiO32-+2H2↑或Al2O3+2OH-=2AlO2-+H2O或SiO2+2OH-=SiO32-+H2O.
(3)步骤⑤中H2O2参加反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)步骤⑥中调节溶液pH时适宜的物质是C、D(填序号).
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
(5)步骤⑦中用硫酸调节pH=2~3的原因是抑制Cu2+的水解,也不会引入杂质.
(6)步骤⑧的分离方法步骤是蒸发浓缩,冷却结晶,过滤,(洗涤、干燥).
13.下列说法正确的是( )
| A. | NaCl晶体中每个钠离子与周围6个氯离子形成6个离子键 | |
| B. | 前四周期元素的原子中,未成对电子数最多的是Mn | |
| C. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| D. | 岩浆冷却过程中,晶格能高的矿物晶体先结晶 |
20.下列说法中正确的是( )
| A. | 1mol任何气体都含有相同的原子数 | |
| B. | 在100℃、1×104Pa时,1mol O2中约含有6.02×1023个O2分子 | |
| C. | 含有阿伏加德罗常数个水分子的水(4℃)其体积为18mL(ρ=1g/cm3) | |
| D. | 两种物质完全反应时,它们的物质的量一定相等 |
3.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次升高 | |
| B. | P、S、Cl元素最高正化合价依次升高 | |
| C. | B、C、N、O、F原 子半径依次升高 | |
| D. | Li、Na、K的原子半径依次增大 |
10.下列有关酸的事实和括号中对应表现出的性质均正确的是( )
| A. | H2S气体能用浓硫酸进行干燥(浓硫酸的吸水性) | |
| B. | 铜与浓硝酸制备NO2气体(浓硝酸的强氧化性、酸性) | |
| C. | SO2的水溶液能够使品红溶液褪色(H2SO3的强氧化性) | |
| D. | 可口可乐瓶盖打开后,有大量气体逸出(H2CO3的挥发性) |
7.在一定条件下,可逆反应2A?B+3C在下列4种状态中,处于平衡状态的是( )
| A. | 正反应速度 vA=2mol/(L•min)逆反应速度vB=2 mol/(L•min) | |
| B. | 正反应速度 vA=2mol/(L•min)逆反应速度vC=2 mol/(L•min) | |
| C. | 正反应速度 vA=1mol/(L•min)逆反应速度vB=1.5 mol/(L•min) | |
| D. | 正反应速度 vA=1mol/(L•min)逆反应速度vC=1.5mol/(L•min) |
8.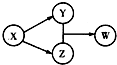 X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
 X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )| A | B | C | D | |
| X | HCl | Na2O2 | Na2CO3 | Al |
| Y | FeCl2 | NaOH | CO2 | Na[Al(OH)4] |
| Z | Cl2 | Na2CO3 | CaCO3 | AlCl3 |
| W | FeCl3 | NaHCO3 | Ca(HCO3)2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |