题目内容
9.在盛有稀 H2SO4 的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )| A. | 正极附近的 SO42- 离子浓度逐渐增大 | |
| B. | 电流由锌片流向铜片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上析出氢气 |
分析 铜-锌-稀硫酸原电池中,活泼金属锌作负极,铜作正极;负极上锌失电子生成锌离子,正极上氢离子得电子生成氢气;溶液中阴离子向负极移动,阳离子向正极移动;由此分析解答.
解答 解:A、该原电池放电时,溶液中阴离子向负极移动,阳离子向正极移动,所以硫酸根离子向负极移动,则负极附近的 SO42- 离子浓度逐渐增大,故A错误;
B、铜-锌-稀硫酸原电池中,活泼金属锌作负极,铜作正极;原电池放电时,电流从正极铜沿导线流向负极锌,故B错误;
C、该原电池中正极上氢离子得电子生成氢气,导致溶液中氢离子浓度降低,pH逐渐变大,故C错误;
D、正极上氢离子得电子生成氢气,所以铜片上有H2逸出,故D正确;
故选:D.
点评 本题考查了原电池原理,难度不大,易错点为:判断溶液中阴阳离子的移动方向.

练习册系列答案
相关题目
19. 如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )
 如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )| A. | 最简单气态氢化物的稳定性③比⑦小 | |
| B. | ①与④能形成原子个数比为1:1的化合物 | |
| C. | ⑤和⑥的最高价氧化物对应的水化物可以反应 | |
| D. | 原子半径②>③>④ |
20.对于mA(气)+nB(气)?pC(气)+qD(气)的平衡体系,当升高温度时,体系对氢气的相对密度从16.5变成16.9,则下列说法正确的是( )
| A. | m+n>p+q 正反应是放热反应 | B. | m+n>p+q 正反应是吸热反应 | ||
| C. | m+n<p+q 逆反应是放热反应 | D. | m+n=p+q 逆反应是吸热反应 |
4.下列物质在水溶液中的电离方程式书写正确的是( )
| A. | CH3COOH?H++CH3COO- | B. | Ba(OH)2 ?Ba2++2OH- | ||
| C. | H3PO4 ?3H++PO${\;}_{4}^{3-}$ | D. | NH3•H2O═NH${\;}_{4}^{+}$+OH- |
14.对下列各组物质关系的描述中不正确的是( )
| A. | O2和O3互为同素异形体 | B. | 1H、2H和3H互为同位素 | ||
| C. | CH2═CH2和 互为同系物 互为同系物 | D. |  和 和 互为同分异构体 互为同分异构体 |
5.将0.1mol•L-1的氨水加水稀释至0.01mol•L-1,稀释过程中温度不变,下列叙述正确的是( )
| A. | 稀释后溶液中的c(H+)和c(OH-)均减小 | |
| B. | 稀释过程中氨水的电离平衡向左移动 | |
| C. | 稀释后溶液中c(OH-)变为稀释前的$\frac{1}{10}$ | |
| D. | 稀释过程中溶液中$\frac{[0{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$增大 |
6.元素周期律(表)是认识元素化合物性质的重要理论.
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈.
ⅱ.锂和镁的氢氧化物均为中等强度的碱.
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物.
由以上事实,可知锂、钠、镁三种元素的金属性强弱关系是Na>Mg=Li.
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族.
①碱性:Sr(OH)2< Ba (OH)2(填“>”或“<”).
②用原子结构的观点解释锶的化学性质与钡差异的原因:锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱.
(3)硒(Se)的部分信息如右图,且知34Se、35Br位于同一周期.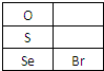
①Se在元素周期表中的位置是第四周期第VIA族.
②H2Se的电子式是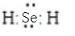 .
.
③Cl、Se、Br的非金属性强弱的顺序是Cl>Br>Se.
能证明上述非金属性强弱关系的事实是氢化物的稳定性(写出一条即可).
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的.
完成下表:
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈.
ⅱ.锂和镁的氢氧化物均为中等强度的碱.
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物.
由以上事实,可知锂、钠、镁三种元素的金属性强弱关系是Na>Mg=Li.
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族.
①碱性:Sr(OH)2< Ba (OH)2(填“>”或“<”).
②用原子结构的观点解释锶的化学性质与钡差异的原因:锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱.
(3)硒(Se)的部分信息如右图,且知34Se、35Br位于同一周期.

①Se在元素周期表中的位置是第四周期第VIA族.
②H2Se的电子式是
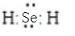 .
.③Cl、Se、Br的非金属性强弱的顺序是Cl>Br>Se.
能证明上述非金属性强弱关系的事实是氢化物的稳定性(写出一条即可).
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的.
完成下表:
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | SeO2+2SO2+2H2O═Se+2H2SO4 |
| 2 | 还原性 | SeO2+2H2O2=H2SeO4+2H2O |
| 3 | 酸性氧化物 | SeO2+NaOH=Na2SeO3+H2O |
 Na2CO3和NaHCO3是两种常见的钠盐.
Na2CO3和NaHCO3是两种常见的钠盐. 中学实验室用如图装置制取少量溴苯,在烧瓶a中装的试剂是苯、液溴和铁粉,d中装的是蒸馏水.请回答下列问题.
中学实验室用如图装置制取少量溴苯,在烧瓶a中装的试剂是苯、液溴和铁粉,d中装的是蒸馏水.请回答下列问题.