题目内容
6.元素周期律(表)是认识元素化合物性质的重要理论.(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈.
ⅱ.锂和镁的氢氧化物均为中等强度的碱.
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物.
由以上事实,可知锂、钠、镁三种元素的金属性强弱关系是Na>Mg=Li.
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族.
①碱性:Sr(OH)2< Ba (OH)2(填“>”或“<”).
②用原子结构的观点解释锶的化学性质与钡差异的原因:锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱.
(3)硒(Se)的部分信息如右图,且知34Se、35Br位于同一周期.
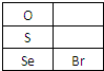
①Se在元素周期表中的位置是第四周期第VIA族.
②H2Se的电子式是
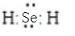 .
.③Cl、Se、Br的非金属性强弱的顺序是Cl>Br>Se.
能证明上述非金属性强弱关系的事实是氢化物的稳定性(写出一条即可).
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的.
完成下表:
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | SeO2+2SO2+2H2O═Se+2H2SO4 |
| 2 | 还原性 | SeO2+2H2O2=H2SeO4+2H2O |
| 3 | 酸性氧化物 | SeO2+NaOH=Na2SeO3+H2O |
分析 (1)金属性越强,其对应最高价氧化物水化物的碱性越强;
(2)同主族,最外层电子数相同,性质相似,从上到下金属性增强;
(3)①Br处于第四周期第VIIA族,Se原子序数比Br小1,据此解答即可;
②为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H-Se键;
③同一主族,原子序数越大,非金属性越弱,同一周期,原子序数越大,非金属性越强,从氢化物的稳定性强弱可以得出非金属性强弱;
④类比二氧化硫的性质回答即可,二氧化硫具有氧化性、还原性和酸性氧化物的性质.
解答 解:(1)由题给信息可知,Na与水反应剧烈,Mg与Li反应不剧烈,Mg与Li均形成中强碱,NaOH为强碱,且Mg与Li只生成氧化物,Na形成过氧化物,据此判断金属性:Na>Mg=Li,故答案为:Na>Mg=Li;
(2)金属性Sr<Ba,则碱性:Sr(OH)2<Ba(OH)2,锶的化学性质与钙和钡类似,是因同一主族元素,原子最外层电子数相同,
故答案为:<; 锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱;
(3)①Br处于第四周期第VIIA族,Se原子序数比Br小1,故处于第四周期第VIA族,故答案为:第四周期第VIA族;
②H2Se为共价化合物,硒原子中最外层有8个电子达到稳定结构,分子中存在两个H-Se键,电子式为: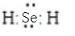 ,故答案为:
,故答案为: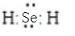 ;
;
③同一主族,原子序数越大,非金属性越弱,同一周期,原子序数越大,非金属性越强,故非极性性:Cl>Br>Se,氢化物的稳定性可以说明此点,即氢化物稳定性顺序为:HCl>HBr>HSe,故答案为:Cl>Br>Se;氢化物的稳定性;
④SeO2与SO2性质类似,二氧化硫具有氧化性、还原性和酸性氧化物的性质,故SeO2也具有这些性质,发生反应分别为SeO2+2H2O2=H2SeO4+2H2O、SeO2+NaOH=Na2SeO3+H2O,
故答案为:还原性;SeO2+2H2O2=H2SeO4+2H2O;酸性氧化物;SeO2+NaOH=Na2SeO3+H2O.
点评 本题考查元素周期律及其应用,学生熟悉元素的金属性与非金属性的递变规律是解答本题的关键,难度不大.

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案| A. | 正极附近的 SO42- 离子浓度逐渐增大 | |
| B. | 电流由锌片流向铜片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上析出氢气 |
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的气态氢化物稳定性比⑦的气态氢化物强.(填“强”、“弱”或“相同”)
(3)由③与⑦形成的化合物的电子式为
 ,①的最高价氧化物的电子式为
,①的最高价氧化物的电子式为 .
.(4)④、⑥、⑧原子半径依次减小(填“增大”、“减小”或“不变”),②、⑤、⑦形成的简单离子半径由大到小顺序为(填离子符号)S2->F->Al3+.
(5)⑥的原子结构示意图为
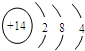 ,其最高价氧化物形成的晶体类型为原子晶体.
,其最高价氧化物形成的晶体类型为原子晶体.(6)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物溶液反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
| A. | C4H10 | B. | C3H8 | C. | C2H6 | D. | CH3Cl |
| A. | 液氯、金刚石都属于单质 | B. | 漂白粉、CuSO4•5H2O都属于混合物 | ||
| C. | 次氯酸、氨气都属于电解质 | D. | 蛋白质、油脂都属于高分子化合物 |
| A. | 该反应属于置换反应 | |
| B. | ${\;}_{\;}^{12}$C和${\;}_{\;}^{14}$C是碳元素的两种同素异形体 | |
| C. | 该反应中化学能全部转化为热能 | |
| D. | 在该反应条件下,C的还原性强于Mg的还原性 |
| A. | 石油分馏可获得石油气、汽油、苯及其同系物等 | |
| B. | 石油催化裂化主要得到乙烯、乙炔等 | |
| C. | 煤含有苯和甲苯,可干馏后获得苯和甲苯 | |
| D. | 煤的液化、气化属于均属于化学变化 |
| A. | 若甲为NH3,则丁可能是O2 | B. | 若甲为AlCl3,则丁可能是NaOH | ||
| C. | 若甲为NaOH溶液,则丁可能是CO2 | D. | 若甲为SiO2,则丁可能是C |