题目内容
5.将0.1mol•L-1的氨水加水稀释至0.01mol•L-1,稀释过程中温度不变,下列叙述正确的是( )| A. | 稀释后溶液中的c(H+)和c(OH-)均减小 | |
| B. | 稀释过程中氨水的电离平衡向左移动 | |
| C. | 稀释后溶液中c(OH-)变为稀释前的$\frac{1}{10}$ | |
| D. | 稀释过程中溶液中$\frac{[0{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$增大 |
分析 一水合氨为弱电解质,加水稀释促进水的电离,将0.1mol•L-1的氨水加水稀释至0.01mol•L-1,c(OH-)减小,但c(H+)增大,由于温度不变,则电离平衡常数k=$\frac{c(NH{\\;}_{4}^{+})×c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不变,以此解答该题.
解答 解:A.稀释后溶液中c(OH-)减小,由于Kw=c(H+)×c(OH-)不变,则c(H+)增大,故A错误;
B.加水稀释促进水的电离,所以电离平衡向右移动,故B错误;
C.一水合氨为弱电解质,加水稀释促进水的电离,稀释后溶液中c(OH-)大于稀释前的$\frac{1}{10}$,故C错误;
D.加水稀释促进水的电离,溶液中n(NH3•H2O)减小,n(OH-)增大,则溶液中$\frac{[0{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$增大,故D正确;故选D.
点评 本题考查弱电解质的电离和水溶液中的电离平衡问题,题目难度不大,注意把握弱电解质的电离特点,能正确判断溶液离子浓度的变化.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列能导电的物质是( )
| A. | 固态NaOH | B. | 酒精 | C. | 液态氯化氢 | D. | NaCl溶液 |
9.在盛有稀 H2SO4 的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
| A. | 正极附近的 SO42- 离子浓度逐渐增大 | |
| B. | 电流由锌片流向铜片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上析出氢气 |
13.下列排列顺序正确的是( )
| A. | 常温下将0.1mol•L-1NH4Cl溶液与0.05mol•L-1NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 常温下物质的量浓度相等的①NH4HSO4②CH3COONH4③NH4Cl三种溶液中c(NH4+):①>③>② | |
| C. | 0.1mol•L-1的NaHA溶液,其pH=11,则溶液中:c(HA-)>c(OH-)>c(A2-)>c(H2A) | |
| D. | 在相同条件下,将足联AgCl加入等体积的①0.01mol•L-1 KCl②0.1mol•L-1 KCl溶液③蒸馏水三种液体中,所能溶解的AgCl质量关系为:①>②>③ |
14.如表是元素周期表的一部分,针对①-⑧元素,填写下列空白.
(1)①的最简单气态氢化物分子的空间构型为正四面体结构.
(2)②的气态氢化物稳定性比⑦的气态氢化物强.(填“强”、“弱”或“相同”)
(3)由③与⑦形成的化合物的电子式为 ,①的最高价氧化物的电子式为
,①的最高价氧化物的电子式为 .
.
(4)④、⑥、⑧原子半径依次减小(填“增大”、“减小”或“不变”),②、⑤、⑦形成的简单离子半径由大到小顺序为(填离子符号)S2->F->Al3+.
(5)⑥的原子结构示意图为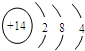 ,其最高价氧化物形成的晶体类型为原子晶体.
,其最高价氧化物形成的晶体类型为原子晶体.
(6)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物溶液反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的气态氢化物稳定性比⑦的气态氢化物强.(填“强”、“弱”或“相同”)
(3)由③与⑦形成的化合物的电子式为
 ,①的最高价氧化物的电子式为
,①的最高价氧化物的电子式为 .
.(4)④、⑥、⑧原子半径依次减小(填“增大”、“减小”或“不变”),②、⑤、⑦形成的简单离子半径由大到小顺序为(填离子符号)S2->F->Al3+.
(5)⑥的原子结构示意图为
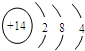 ,其最高价氧化物形成的晶体类型为原子晶体.
,其最高价氧化物形成的晶体类型为原子晶体.(6)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物溶液反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
15.下列关于化石燃料的说法正确的是( )
| A. | 石油分馏可获得石油气、汽油、苯及其同系物等 | |
| B. | 石油催化裂化主要得到乙烯、乙炔等 | |
| C. | 煤含有苯和甲苯,可干馏后获得苯和甲苯 | |
| D. | 煤的液化、气化属于均属于化学变化 |
 ;
; ;
; +2Ag+3NH3+H2O;
+2Ag+3NH3+H2O; .
.