题目内容
17. Na2CO3和NaHCO3是两种常见的钠盐.
Na2CO3和NaHCO3是两种常见的钠盐.(1)下列关于Na2CO3和NaHCO3性质的说法中,正确的是
bd(填字母).a.常温下,Na2CO3在水中的溶解度比NaHCO3小
b.Na2CO3溶液和NaHCO3溶液均显碱性
c.可用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
d.等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2的体积相同
(2)实验室利用图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答:
物质A是Na2CO3(填化学式),写出其中一种物质受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(3)若要除去碳酸氢钠溶液中的碳酸钠,请用化学方程式表示除杂原理Na2CO3+CO2+H2O=2NaHCO3.
分析 (1)碳酸钠的溶解度大于碳酸氢钠;碳酸钠和碳酸氢钠溶液都呈碱性;氢氧化钙能够与碳酸钠、碳酸氢钠溶液反应生成碳酸钙沉淀;物质的量相等的碳酸钠和碳酸氢钠含有相同的C原子,根据碳原子守恒可知,等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应生成相同条件下等体积的二氧化碳;
(2)套管实验时,为便于比较稳定度,易分解的物质应在小试管中;碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水;
(3)碳酸钠能够与二氧化碳反应生成碳酸氢钠,据此可除去碳酸氢钠溶液中的碳酸钠.
解答 解:(1)a.常温下,Na2CO3在水中的溶解度比NaHCO3大,故a错误;
b.碳酸根离子、碳酸氢根离子在溶液中发生水解反应,则Na2CO3溶液和NaHCO3溶液均显碱性,故b正确;
c.碳酸钠和碳酸氢钠都能够与氢氧化钙反应生成沉淀,不能Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液,故c错误;
d.根据碳原子守恒可知,等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2的体积相同,故d正确;
故答案为:bd;
(2)套管实验时,为便于比较稳定度,易分解的物质应在小试管中,即B中加入NaHCO3,A中加入Na2CO3,从而说明NaHCO3能在较低温度下分解,反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案为:Na2CO3;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(3)除去碳酸氢钠溶液中的碳酸钠,可向碳酸氢钠溶液中通入过量二氧化碳,将碳酸钠转化成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3,
故答案为:Na2CO3+CO2+H2O=2NaHCO3.
点评 本题考查碳酸钠、碳酸氢钠的稳定性,题目难度中等,侧重实验探究及装置的考查,明确物质的性质及气密性检验、对比作用为解答的关键,试题培养了学生的分析能力及化学实验能力.

| A. | 向空气中大量排放SO2和NO2都能引起酸雨和光化学烟雾 | |
| B. | 不法分子制作假鸡蛋用的海藻酸钠、氯化钙以及碳酸钙都属于盐 | |
| C. | 明矾用于净水既与盐类的水解有关,又与胶体的性质有关 | |
| D. | FeS难溶于水(Ksp=6.3×10-18),但能除去水中的Cu2+(CuS的Ksp=1.3×10-36) |
| A. | 固态NaOH | B. | 酒精 | C. | 液态氯化氢 | D. | NaCl溶液 |
| A. | 1:2:3 | B. | 6:3:2 | C. | 3:2:2 | D. | 3:1:1 |
| A. | c(HPO42-)>c(H3PO4) | B. | c(Na+)+c(H+)=0.1mol•L-1 | ||
| C. | c(Na+)=c(H2PO4-)+c(HPO42-)+C(H3PO4) | D. | 加水稀释后,n(H+)与n(OH-)的乘积不变 |

| A. | 当该卤代烃发生水解反应时,被破坏的键是①和③ | |
| B. | 当该卤代烃发生水解反应时,被破坏的键是① | |
| C. | 当该卤代烃发生消去反应时,被破坏的键是①和④ | |
| D. | 当该卤代烃发生消去反应时,被破坏的键是①和③ |
| A. | 正极附近的 SO42- 离子浓度逐渐增大 | |
| B. | 电流由锌片流向铜片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上析出氢气 |
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的气态氢化物稳定性比⑦的气态氢化物强.(填“强”、“弱”或“相同”)
(3)由③与⑦形成的化合物的电子式为
 ,①的最高价氧化物的电子式为
,①的最高价氧化物的电子式为 .
.(4)④、⑥、⑧原子半径依次减小(填“增大”、“减小”或“不变”),②、⑤、⑦形成的简单离子半径由大到小顺序为(填离子符号)S2->F->Al3+.
(5)⑥的原子结构示意图为
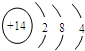 ,其最高价氧化物形成的晶体类型为原子晶体.
,其最高价氧化物形成的晶体类型为原子晶体.(6)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物溶液反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.